
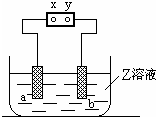
| a极板 | b极板 | X电极 | Z溶液 | |
| A | 石墨 | 石墨 | 正极 | NaOH |
| B | 铜 | 石墨 | 负极 | CuCl2 |
| C | 锌 | 石墨 | 负极 | CuSO4 |
| D | 银 | 铁 | 正极 | AgNO3 |
| A. | A | B. | B | C. | C | D. | D |
分析 X、Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无味气体放出,说明a为阴极、b为阳极,溶液中的阳离子氧化性大于氢离子,阳极上生成氧气说明氢氧根离子放电,X为负极,据此分析解答.
解答 解:X、Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色、无臭气体放出,说明a为阴极、b为阳极,溶液中的阳离子氧化性大于氢离子,阳极上生成氧气说明氢氧根离子放电,X为负极,
A.X为负极而不是正极,故A错误;
B.以石墨为电极电解CuCl2溶液时,a电极上生成铜,b电极上生成氯气为黄绿色,不符合条件,故B错误;
C.以石墨电极材料为电极时电解硫酸铜溶液,a电极上生成铜、b电极上生成氧气,符合条件,故C正确;
D..X为负极而不是正极,故D错误;
故选C.
点评 本题考查电解原理,明确离子放电顺序是解本题关键,知道各个电极上发生的反应,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;
;
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 外,还含有的官能团名称是碳碳双键和酯基;
外,还含有的官能团名称是碳碳双键和酯基; .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光纤的主要成分是高纯度的单质硅 | |
| B. | SiO2是酸性氧化物,它不溶于水也不溶于任何酸 | |
| C. | 因高温时SiO2与Na2CO3反应放出CO2,所以H2SiO3酸性比H2CO3强 | |
| D. | 28Si、29Si、30Si互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
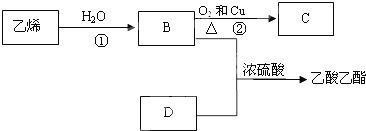

 反应类型:加聚反应.
反应类型:加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上常用MnO2和浓盐酸共热来制取氯气 | |
| B. | 新制氯水可使蓝色石蕊试纸先变红后褪色 | |
| C. | 在氧化还原反应中,Cl2只能作氧化剂 | |
| D. | 若提供含0.4 mol HCl的浓盐酸,MnO2过量,则可制得标准状况下氯气2.24 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com