
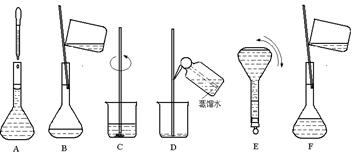
| A��ʹ������ƿǰ������Ƿ�©ˮ |
| B������ƿ������ˮϴ�������ô���Һ��ϴ |
| C�����ݺ�����ƿ��,��ʳָ��סƿ��,����һֻ�ֵ���ָ��סƿ��,������ƿ��תҡ�� |
| D����ȷ��ȡ��18.4 mol��L��1�����ᣬע����ʢ��30 mLˮ��100 mL������ƿ�У���ˮ���̶��� |
 ��V=5.4��
��V=5.4�� ������n��V�ı仯��
������n��V�ı仯��

 �ƸԹھ��ο���ϵ�д�
�ƸԹھ��ο���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.500 mol/L | B��1. 00 mol/L | C��2. 00 mol/L | D��3. 00 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��32g O2�к��еķ�����ΪNA |
| B����״���£�22.4 L H2O�к��еķ�����ΪNA |
| C��1 mol Mg������O2��Ӧת�Ƶĵ�����ΪNA |
| D��1 L 1 mol��L��1 CaCl2��Һ�к��е���������ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����״���£�22.4LCH4��CH3Cl�Ļ���������еķ�����ĿΪNA |
| B��7.8g Na2O2�����к���������������Ϊ0.4NA |
| C��1 mol SiO2�������4NA Si�CO�� |
| D��1.4 g��ϩ(C2H4)�ͱ�ϩ(C3H6)�Ļ�����к�̼�����Ϊ0.2 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����1.0molFeCl3ȫ���Ƴɽ��壬����������������ΪNA�� |
| B�� 0.1molOH����NA������ |
| C��1.8g��ˮ��D2O���к�NA������ |
| D����״����11.2L�����к�NA����ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��7:1 | B��1:7 | C��7:8 | D��8:7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com