
 ¶ĢÖÜĘŚŌŖĖŲT”¢Q”¢R”¢W”¢ZŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēÓŅĶ¼ĖłŹ¾£¬ĘäÖŠTĖł“¦µÄÖÜĘŚŠņŹżÓėÖ÷×åŠņŹżĻąµČ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
¶ĢÖÜĘŚŌŖĖŲT”¢Q”¢R”¢W”¢ZŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēÓŅĶ¼ĖłŹ¾£¬ĘäÖŠTĖł“¦µÄÖÜĘŚŠņŹżÓėÖ÷×åŠņŹżĻąµČ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ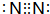
·ÖĪö øł¾Ż¶ĢÖÜĘŚŌŖĖŲQ”¢R”¢T”¢WŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆÖŖ£¬Q”¢R”¢WĪ»ÓŚµŚ¶žÖÜĘŚ£¬TŗĶZĪ»ÓŚµŚČżÖÜĘŚ£¬TĖł“¦µÄÖÜĘŚŠņŹżÓėÖ÷×åŠņŹżĻąµČ£¬ŌņTŹĒAlŌŖĖŲ£¬æÉĶĘÖŖQŹĒCŌŖĖŲ”¢RŹĒNŌŖĖŲ”¢WŹĒOŌŖĖŲ”¢TĪŖCl£®
£Ø1£©QµÄĘųĢ¬Ēā»ÆĪļĪŖ¼×Ķ飬Rµ„ÖŹĪŖN2£¬·Ö×ÓÖŠNŌ×ÓÖ®¼äŠĪ³É3¶Ō¹²ÓƵē×Ó¶Ō£»
£Ø2£©µ„ÖŹČܽāŠŌ£¬ŹōÓŚĪļĄķŠŌÖŹ£¬²»ÄÜ±Č½ĻŌŖĖŲ·Ē½šŹōŠŌĒæČõ£¬æÉŅŌøł¾ŻĒā»ÆĪļĪČ¶ØŠŌ”¢×īøß¼Ūŗ¬ŃõĖįµÄĖįŠŌĒæČõ±Č½Ļ£»
£Ø3£©ĀČ»ÆĀĮČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗ£¬æŖŹ¼Éś³ÉĒāŃõ»ÆĀĮ³Įµķ£¬¶ųŗóĒāŃõ»ÆĀĮÓėĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĘ«ĀĮĖįÄĘÓėĖ®£¬³ĮµķÓÖČܽā£»
£Ø4£©CO ŗĶNO¶¼ŹĒĘū³µĪ²ĘųÖŠŗ¬ÓŠµÄ“óĘųĪŪČ¾Īļ£¬ŌŚĘū³µÅÅĘų¹ÜµÄ”°“ß»Æ×Ŗ»»Ę÷”±ÖŠ·“Ӧɜ³ÉæɲĪÓė“óĘųÉśĢ¬Ń»·µÄĪŽ¶¾ĘųĢ壬ӦŹĒÉś³ÉµŖĘųÓė¶žŃõ»ÆĢ¼£»
£Ø5£©MŹĒŅ»ÖÖ³£¼ūµÄ½šŹōµ„ÖŹ£¬ÓÉ×Ŗ»Æ¹ŲĻµæÉÖŖ£¬ĪŖ±ä¼Ū½šŹō£¬æÉĶĘÖŖMĪŖFe”¢EĪŖFeCl3”¢FĪŖFeCl2£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗ¶ĢÖÜĘŚŌŖĖŲT”¢Q”¢R”¢W”¢ZŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆæÉÖŖ£¬T”¢Z“¦ÓŚµŚČżÖÜĘŚ£¬Q”¢R”¢W“¦ÓŚµŚ¶žÖÜĘŚ£¬TĖł“¦µÄÖÜĘŚŠņŹżÓėÖ÷×åŠņŹżĻąµČ£¬ŌņZĪŖAl£¬æÉĶĘÖŖQĪŖC”¢RĪŖN”¢WĪŖO”¢ZĪŖCl£¬
£Ø1£©Q µÄĘųĢ¬Ēā»ÆĪļ¼×ĪŖ¼×Ķ飬»ÆѧŹ½ĪŖCH4£¬Rµ„ÖŹĪŖN2£¬·Ö×ÓÖŠNŌ×ÓÖ®¼äŠĪ³É3¶Ō¹²ÓƵē×Ó¶Ō£¬µē×ÓŹ½ĪŖ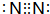 £¬
£¬
¹Ź“š°øĪŖ£ŗCH4£»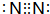 £»
£»
£Ø2£©¢Łµ„ÖŹČܽāŠŌ£¬ŹōÓŚĪļĄķŠŌÖŹ£¬²»ÄÜ±Č½ĻŌŖĖŲ·Ē½šŹōŠŌĒæČõ£¬¹Ź¢Ł“ķĪó£»
¢ŚŌŖĖŲ×īøß¼Ūŗ¬ŃõĖįµÄĖįŠŌŌ½Ē棬ŌŖĖŲ·Ē½šŹōŠŌŌ½Ē棬¹Ź¢ŚÕżČ·£»
¢ŪŌŖĖŲĒā»ÆĪļŌ½ĪČ¶Ø£¬ĖµĆ÷øĆŌŖĖŲ·Ē½šŹōŠŌŌ½Ē棬¹Ź¢ŪÕżČ·£»
¹Ź“š°øĪŖ£ŗ¢Ś¢Ū£»
£Ø3£©ĀČ»ÆĀĮČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗ£¬æŖŹ¼Éś³ÉĒāŃõ»ÆĀĮ³Įµķ£¬¶ųŗóĒāŃõ»ÆĀĮÓėĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĘ«ĀĮĖįÄĘÓėĖ®£¬³ĮµķÓÖČܽā£¬³ĮµķČܽāµÄĄė×Ó·½³ĢŹ½£ŗAl£ØOH£©3+OH-=AlO2-+2H2O£¬
¹Ź“š°øĪŖ£ŗAl£ØOH£©3+OH-=AlO2-+2H2O£»
£Ø4£©CO ŗĶNO¶¼ŹĒĘū³µĪ²ĘųÖŠŗ¬ÓŠµÄ“óĘųĪŪČ¾Īļ£¬ŌŚĘū³µÅÅĘų¹ÜµÄ”°“ß»Æ×Ŗ»»Ę÷”±ÖŠ·“Ӧɜ³ÉæɲĪÓė“óĘųÉśĢ¬Ń»·µÄĪŽ¶¾ĘųĢ壬ӦŹŹŹ±µŖĘųÓė¶žŃõ»ÆĢ¼£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗ2CO+2NO$\frac{\underline{\;“߻ƼĮ\;}}{\;}$N2+2CO2£¬
¹Ź“š°øĪŖ£ŗ2CO+2NO$\frac{\underline{\;“߻ƼĮ\;}}{\;}$N2+2CO2£»
£Ø5£©MŹĒŅ»ÖÖ³£¼ūµÄ½šŹōµ„ÖŹ£¬ÓÉ×Ŗ»Æ¹ŲĻµæÉÖŖ£¬MĪŖ±ä¼Ū½šŹō£¬æÉĶĘÖŖMĪŖFe”¢EĪŖFeCl3”¢FĪŖFeCl2£¬Ōņ£ŗ
¢ŁE×Ŗ»ÆĪŖFµÄ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ£ŗFe3++2Fe=3Fe2+£¬¹Ź“š°øĪŖ£ŗFe3++2Fe=3Fe2+£»
¢ŚÓĆKSCNČÜŅŗ¼ģŃéFeCl3ČÜŅŗÖŠĢśĄė×Ó£¬¹Ź“š°øĪŖ£ŗKSCNČÜŅŗ£»
¢ŪFeCl2ČÜŅŗÖŠ×ćĮæµÄĒāŃõ»ÆÄĘŗó£¬æŖŹ¼Éś³ÉĒāŃõ»ÆŃĒĢś³Įµķ£¬ŃøĖŁ±»Ńõ»ÆĪŖĒāŃõ»ÆĢś£¬ŹŌ¹ÜÖŠµÄĻÖĻóŹĒ£ŗæŖŹ¼²śÉś°×É«³Įµķ£¬ŃøĖŁ±äĪŖ»ŅĀĢÉ«£¬×īÖÕ±äĪŖŗģŗÖÉ«³Įµķ£¬
¹Ź“š°øĪŖ£ŗæŖŹ¼²śÉś°×É«³Įµķ£¬ŃøĖŁ±äĪŖ»ŅĀĢÉ«£¬×īÖÕ±äĪŖŗģŗÖÉ«³Įµķ£®
µćĘĄ ±¾Ģāæ¼²é½į¹¹ŠŌÖŹĪ»ÖĆ¹ŲĻµ”¢ĪŽ»śĪļĶʶĻ£¬ĶʶĻŌŖĖŲŹĒ½āĢā¹Ų¼ü£¬×ŪŗĻæ¼²éѧɜ¶ŌÖŖŹ¶µÄĒØŅĘŌĖÓĆÄÜĮ¦£¬×¢ŅāÕĘĪÕ½šŹōŠŌ”¢·Ē½šŹōŠŌĒæČõ±Č½ĻŹµŃéŹĀŹµ£¬ÄѶČÖŠµČ£®


 ø÷µŲĘŚÄ©ø“Ļ°ĢŲѵ¾ķĻµĮŠ“š°ø
ø÷µŲĘŚÄ©ø“Ļ°ĢŲѵ¾ķĻµĮŠ“š°ø Š”²©ŹæĘŚÄ©“³¹Ų100·ÖĻµĮŠ“š°ø
Š”²©ŹæĘŚÄ©“³¹Ų100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĶØČėCO2¹ż³ĢÖŠČÜŅŗµÄKw¼õŠ” | |
| B£® | µ±b=0.2Ź±£¬ĖłµĆČÜŅŗÖŠ²æ·ÖĄė×ÓÅØ¶Č¹ŲĻµĪŖ£ŗc £ØHCO3-£©£¾c £ØCO32-£©£¾c £Ø OH-£©£¾c £ØH+£© | |
| C£® | b=0.3Óėb=0.15Ź±£¬ĖłµĆČÜŅŗÖŠµÄĪ¢Į£ÖÖĄą²»ĻąĶ¬ | |
| D£® | µ±Ē”ŗĆÉś³ÉNaHCO3Ź±£¬ČÜŅŗÖŠ“ęŌŚ£ŗc£ØNa+£©+c£ØH+£©ØTc£ØHCO3-£©+c£Ø OH-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SiO2²»ÄÜÓėHNO3”¢H2SO4µČĖłÓŠµÄĖį·“Ó¦ | |
| B£® | CO2ŗĶSiO2µÄ¶ŌÓ¦Ė®»ÆĪļ¶¼ŹĒĖį£¬Ģ¼ĖįĖįŠŌ±Č¹čĖįČõ | |
| C£® | CO2ÓėSiO2¾łŹĒĖįŠŌŃõ»ÆĪļ£¬ČÜÓŚĖ®¾łµĆµ½ĻąÓ¦µÄĖį | |
| D£® | ¹č½ŗ³£ÓĆÓŚ×öøÉŌļ¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗX£¼Z | |
| B£® | Ō×Ó°ė¾¶£ŗW£¾Y£¾Z£¾X | |
| C£® | ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄ¼īŠŌ£ŗY£¾W | |
| D£® | Y”¢ZµÄŃõ»ÆĪļ¶¼ÓŠĖįŠŌŗĶ¼īŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CuSO4 | B£® | CuO | C£® | CuSO4•5H2O | D£® | Cu£ØOH£©2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃéŠņŗÅ | ŹµŃé²½ÖčŗĶ²Ł×÷ | ŹµŃéĻÖĻó |
| ŹµŃéŅ» | £Ø¢ń£©Č”ĀČ»ÆŃĒĢś¹ĢĢå[ŅŃ²æ·Ö±äÖŹ£¬ŗ¬ÓŠÉŁĮæÄŃČÜÓŚĖ®µÄŌÓÖŹFe£ØOH£©2Cl]£¬ĻņĘäÖŠ¼ÓČė¹żĮæĻ”ŃĪĖį£® £Ø¢ņ£©ŌŁ¼ÓČėÉŌ¹żĮæµÄĢś·Ū£¬Õńµ“£® | ¹ĢĢåĶźČ«Čܽā£¬ČÜŅŗ³Ź»ĘĀĢÉ« Fe£ØOH£©2Cl+2H+=Fe3++Cl-+2H2O |
| ŹµŃ鶞 | £Ø¢ń£©Č”ŹµŃéŅ»µĆµ½µÄČÜŅŗ£¬¼ÓČėKSCNČÜŅŗ£® £Ø¢ņ£©ŌŁ¼ÓČėÉŁĮæH2O2ČÜŅŗ£® | ŃÕÉ«ĪŽĆ÷ĻŌ±ä»Æ ČÜŅŗ±äŗģ£¬ÓŠÉŁĮæĘųÅŻ |
| ŹµŃéČż | £Ø¢ń£©Č”10mL 0.1mol/L KIČÜŅŗ£¬µĪ¼Ó6µĪ0.1mol/L FeCl3ČÜŅŗ£® £Ø¢ņ£©Č”ÉŁĮæÉĻŹö»ĘÉ«ČÜŅŗ£¬µĪ¼ÓKSCNČÜŅŗ£® £Ø¢ó£©ĮķČ”ÉĻŹöµÄ»ĘÉ«ČÜŅŗ£¬¼ÓČėµķ·ŪČÜŅŗ£® | ČÜŅŗ³Ź»ĘÉ« ČÜŅŗ±äŗģ ČÜŅŗ±äĄ¶ |
| ŹµŃéĖÄ | £Ø¢ń£©ĻņŹµŃéČż²½ÖčIÖŠĖłµĆµÄ»ĘÉ«ČÜŅŗÖŠ¼ÓČė2mL CCl4£¬³ä·ÖÕńµ“ŗó£¬·ÖĄėµĆµ½Ė®²ć£»ÖŲø“²Ł×÷Čż“Ī£® £Ø¢ņ£©Ļņ²½ÖčIÖŠĖłµĆĖ®²ćÖŠ¼ÓČėKSCNČÜŅŗ£® | ŃÕÉ«ĪŽĆ÷ĻŌ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ijĶ¬Ń§ĄūÓĆĶ¼½ųŠŠÅēČŖŹµŃ飬ŅŃÖŖŌ²µ×ÉÕĘæÄŚ³äĀśXĘųĢ壬½ŗĶ·µĪ¹ÜČװӊɣĮæYŅŗĢ壬ÉÕ±ÄŚ×°ÓŠ×ćĮæZŅŗĢ壬ĻĀĮŠ×éŗĻÄܽųŠŠÅēČŖŹµŃéĒŅ×īÖÕŅŗĢåŅ»¶ØÄܳäĀśÕūøöÉÕĘæµÄŹĒ£Ø””””£©
ijĶ¬Ń§ĄūÓĆĶ¼½ųŠŠÅēČŖŹµŃ飬ŅŃÖŖŌ²µ×ÉÕĘæÄŚ³äĀśXĘųĢ壬½ŗĶ·µĪ¹ÜČװӊɣĮæYŅŗĢ壬ÉÕ±ÄŚ×°ÓŠ×ćĮæZŅŗĢ壬ĻĀĮŠ×éŗĻÄܽųŠŠÅēČŖŹµŃéĒŅ×īÖÕŅŗĢåŅ»¶ØÄܳäĀśÕūøöÉÕĘæµÄŹĒ£Ø””””£©| XĘųĢå | YŹŌ¼Į | ZŹŌ¼Į | |
| A£® | NO2 | H2O | H2O |
| B£® | CO2 | H2O | H2O |
| C£® | HCl | ±„ŗĶŹ³ŃĪĖ® | Ė® |
| D£® | NO2ŗĶO2 | H2O | H2O |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com