
| A、氯气溶于水:Cl2+H20═2H++C1-+C10- |
| B、硫酸铝溶液中加入足量氨水:Al3++40H-═[Al(OH)4]- |
| C、大理石溶于醋酸中:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O |
| D、碳酸钠溶液水解的离子方程式:CO32-+2H2O?H2CO3+2OH- |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 3 |
| 2 |
| 3 |
| 1 |
| 3 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| △ |
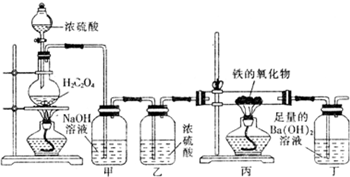
查看答案和解析>>
科目:高中化学 来源: 题型:
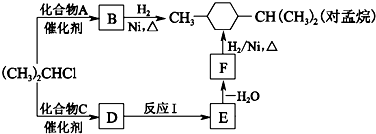
 (R为烷基,X为卤素原子)②RCH2CH2OH
(R为烷基,X为卤素原子)②RCH2CH2OH| H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com