
XΓΔYΓΔZΓΔQΓΔR «Έε÷÷ΕΧ÷ήΤΎ‘ΣΥΊΘ§‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΓΘXΓΔYΝΫ‘ΣΥΊΉνΗΏ’ΐΦέ”κΉνΒΆΗΚΦέ÷°ΚΆΨυΈΣ0ΘΜQ”κXΆ§÷ςΉεΘΜZΓΔRΖ÷±π «ΒΊΩ«÷–Κ§ΝΩΉνΗΏΒΡΖ«Ϋπ τ‘ΣΥΊΚΆΫπ τ‘ΣΥΊΓΘ«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©Έε÷÷‘ΣΥΊ‘≠Ή”ΑκΨΕ”…¥σΒΫ–ΓΒΡΥ≥–ρ «Θ®–¥‘ΣΥΊΖϊΚ≈Θ©_________________________ΓΘ
Θ®2Θ©QXΒΡΒγΉ” ΫΈΣ___________ΘΜQX”κΥ°Ζ¥”ΠΖ≈≥ωΤχΧεΒΡΜ·―ßΖΫ≥Χ ΫΈΣ____________ΓΘ
Θ®3Θ©XΓΔZΝΫ‘ΣΥΊΡή–Έ≥…ΝΫ÷÷Μ·ΚœΈοΒΡΒγΉ” ΫΖ÷±πΈΣ ΚΆ ΓΓΓΓΓΘ
Θ®4Θ©”…“‘…œΡ≥–©‘ΣΥΊΉι≥…ΒΡΜ·ΚœΈοAΓΔBΓΔCΓΔD”–»γœ¬ΉΣΜ·ΙΊœΒ

Τδ÷–C «»ή”ΎΥ°œ‘Υα–‘ΒΡΤχΧεΘΜD «Β≠ΜΤ…ΪΙΧΧεΓΘ
ΔΌ –¥≥ωCΒΡΫαΙΙ Ϋ__________________ΘΜ
ΔΎ »γΙϊAΓΔBΨυ”…»ΐ÷÷‘ΣΥΊΉι≥…Θ§BΈΣΝΫ–‘≤Μ»ήΈοΘ§”…AΉΣΜ·ΈΣBΒΡάκΉ”ΖΫ≥Χ Ϋ
__ ___ __ΓΘ

| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
œ¬Ν–Ζ¥”Π÷–Θ§≤Μ τ”Ύ―θΜ·ΜΙ‘≠Ζ¥”ΠΒΡ «( )
AΘ°2H2O2 MnO2 2H2O + O2Γϋ
BΘ°NH4Cl Γς NH3Γϋ + HClΓϋ
CΘ°2Al + Fe2O3 ΗΏΈ¬ 2Fe + Al2O3
DΘ°Cu + 2H2SO4(≈®) Γς CuSO4 + SO2Γϋ + 2H2O
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
œ¬Ν–Έο÷ ΘΚΔΌH2 ΔΎHF ΔέH2O2 ΔήKF ΔίNH4Cl ΔόC2H2 ΔΏN2H4+ ΔύBF3 ΔαH2O ΔβN2Θ®Χν–ρΚ≈Θ©
Θ®1Θ©÷ΜΚ§Ζ«ΦΪ–‘ΦϋΒΡ «___________________ Θ®2Θ©÷ΜΚ§ΦΪ–‘ΦϋΒΡΦΪ–‘Ζ÷Ή” «_____________
Θ®3Θ©Φ»”–ΦΪ–‘Φϋ”÷”–Ζ«ΦΪ–‘ΦϋΒΡ «_________ Θ®4Θ©÷Μ”–Π“ΦϋΒΡ «_______________________
Θ®5Θ©Φ»”–Π“Φϋ”÷”–Π–ΦϋΒΡ «_______________ Θ®6Θ©Κ§”–≈δΈΜΦϋΒΡ «_____________________
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
“―÷ΣΘΚ
2H2(g)ΘΪO2(g)===2H2O(l) ΠΛHΘΫΘ≠571.6 kJΓΛmolΘ≠1
2CH3OH(l)ΘΪ3O2(g)===2CO2(g)ΘΪ4H2O(l) ΠΛHΘΫΘ≠1452 kJΓΛmolΘ≠1
HΘΪ(aq)ΘΪOHΘ≠(aq)===H2O(l) ΠΛHΘΫΘ≠57.3 kJΓΛmolΘ≠1
œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «ΘΚ
AΘ°H2(g)ΒΡ»Φ…’»»ΈΣ571.6 kJΓΛmolΘ≠1
BΘ°Ά§÷ ΝΩΒΡH2(g)ΚΆCH3OH(l)Άξ»Ϊ»Φ…’Θ§H2(g)Ζ≈≥ωΒΡ»»ΝΩΕύ
CΘ°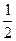 H2SO4(aq)ΘΪ
H2SO4(aq)ΘΪ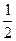 Ba(OH)2(aq)===
Ba(OH)2(aq)===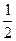 BaSO4(s)ΘΪH2O(l) ΠΛHΘΫΘ≠57.3 kJΓΛmolΘ≠1
BaSO4(s)ΘΪH2O(l) ΠΛHΘΫΘ≠57.3 kJΓΛmolΘ≠1
DΘ°3H2(g)ΘΪCO2(g)=CH3OH(l)ΘΪH2O(l) ΠΛHΘΫΘΪ135.9 kJΓΛmolΘ≠1
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
œ¬Ν–±μ ΨΕ‘”ΠΜ·―ßΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ’ΐ»ΖΒΡ «ΘΚ
AΘ° ΫΪΙΐΝΩSO2ΤχΧεΆ®»κΑ±Υ°÷–ΘΚSO2+2 NH3ΓΛH2O =2 NH4+ + SO32Θ≠+H2O
BΘ° œρFeI2»ή“Κ÷–Ά®»κΉψΝΩΒΡ¬»ΤχΘΚ2Fe2ΘΪΘΪ2IΘ≠ΘΪ2Cl2===2Fe3ΘΪΘΪI2ΘΪ4ClΘ≠
CΘ° œρ«β―θΜ·±Β»ή“Κ÷–÷πΒΈΦ”»κ…ΌΝΩΧΦΥα«βΡΤ»ή“ΚΘΚ
Ba2++2OH-+2HCO3- = BaCO3Γΐ+2H2O+ CO32-
DΘ° œθΥαΧζ»ή“Κ÷–ΒΈΦ”ΉψΝΩHI»ή“ΚΘΚFe3+ + 3NO3Θ≠+12H+ +10IΘ≠ = Fe2+ + 5I2 + 3NOΓϋ + 6H2O
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
Έο÷ ΒΡΝΩ≈®Ε»œύΆ§ΒΡ»ΐ÷÷’ΐ―ΈNaXΓΔNaYΓΔNaZΒΡΥ°»ή“ΚΘ§ΤδpHΖ÷±πΈΣ8ΓΔ9ΓΔ10Θ§‘ρHXΓΔHYΓΔHZΒΡΥα
–‘”…«ΩΒΫ»θΒΡΥ≥–ρ «Θ® Θ©
AΓΔHX>HZ>HY BΓΔHZ>HY>HZ CΓΔHX>HY>HZ DΓΔHY>HZ>HX
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
Μ·―ß”Ο”ο «―ßœΑΜ·―ßΒΡ÷Ί“ΣΙΛΨΏ,œ¬Ν–”Οά¥±μ ΨΈο÷ ±δΜ·ΒΡΜ·―ß”Ο”ο÷–,’ΐ»ΖΒΡ «Θ® Θ©
A.¬»ΦνΙΛ“Β÷–ΒγΫβ±ΞΚΆ ≥―ΈΥ° ±,―τΦΪΒΡΒγΦΪΖ¥”ΠΈΣ:2Cl--2e- Cl2Γϋ
Cl2Γϋ
B.«β―θ»ΦΝœΒγ≥ΊΒΡΗΚΦΪΖ¥”Π:O2+2H2O+4e- 4OH-
4OH-
C.¥÷Ά≠ΨΪΝΕ ±,”κΒγ‘¥’ΐΦΪœύΝ§ΒΡ «¥ΩΆ≠,ΒγΦΪΖ¥”ΠΈΣ:Cu-2e- Cu2+
Cu2+
D.Η÷ΧζΖΔ…ζΒγΜ·―ßΗ· ¥ΒΡ’ΐΦΪΖ¥”Π:Fe-2e- Fe2+
Fe2+
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «(ΓΓΓΓ)
AΘ°ΟΚΒΡ“ΚΜ·ΚΆΤχΜ·ΕΦ «Έοάμ±δΜ·
BΘ°““¥ΦΓΔ““ΥαΚΆΦΉ»©ΙψΖΚ”Π”Ο”Ύ ≥ΤΖΦ”ΙΛ
CΘ°ΒΑΑΉ÷ ΓΔœπΫΚΚΆΥήΝœΕΦ «Χλ»ΜΗΏΖ÷Ή”
DΘ°ΗΏΧζ≥Βœα¥σ≤ΩΖ÷≤ΡΝœ≤…”Ο¬ΝΚœΫπΘ§“ρ¬ΝΚœΫπ«ΩΕ»¥σΓΔ÷ ΝΩ«αΓΔΩΙΗ· ¥ΡήΝΠ«Ω
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΆιΜυ»Γ¥ζ±Ϋ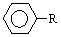 Ω…±ΜΥα–‘ΗΏΟΧΥαΦΊ»ή“Κ―θΜ·ΈΣ
Ω…±ΜΥα–‘ΗΏΟΧΥαΦΊ»ή“Κ―θΜ·ΈΣ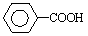 Θ®±ΫΦΉΥαΘ©Θ§ΒΪ»τΆιΜυR÷–÷±Ϋ””κ±ΫΜΖœύΝ§Ϋ”ΒΡΧΦ‘≠Ή”…œΟΜ”–CΘ≠HΦϋΘ§‘ρ≤Μ»ί“Ή±Μ―θΜ·ΒΟΒΫ±ΫΦΉΥαΓΘΨί¥Υ≈–ΕœΘ§Ζ÷Ή” ΫΈΣC11H16ΒΡ“ΜΆιΜυ»Γ¥ζ±ΫΘ§Ω…“‘±Μ―θΜ·ΈΣ±ΫΦΉΥαΒΡ“λΙΙΧεΙ≤”–
Θ®±ΫΦΉΥαΘ©Θ§ΒΪ»τΆιΜυR÷–÷±Ϋ””κ±ΫΜΖœύΝ§Ϋ”ΒΡΧΦ‘≠Ή”…œΟΜ”–CΘ≠HΦϋΘ§‘ρ≤Μ»ί“Ή±Μ―θΜ·ΒΟΒΫ±ΫΦΉΥαΓΘΨί¥Υ≈–ΕœΘ§Ζ÷Ή” ΫΈΣC11H16ΒΡ“ΜΆιΜυ»Γ¥ζ±ΫΘ§Ω…“‘±Μ―θΜ·ΈΣ±ΫΦΉΥαΒΡ“λΙΙΧεΙ≤”–
A. 6÷÷ B. 7÷÷ C. 8÷÷ D. 9÷÷
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com