
下列叙述正确的是( )
A.离子晶体中,只存在离子键,不可能存在其他化学键
B.在氧族元素(O、S、Se、Te)的氢化物中,水的沸点最低
C.NaHSO4、Na2O2晶体中的阴阳离子个数比均为1∶2
D.晶体的熔点:金刚石>碳化硅>单晶硅
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。
(1)工业上用黄铁矿(FeS2,其中硫元素为-1价)在高温下和氧气反应制备SO2:4FeS2+11O2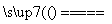 8SO2+2Fe2O3,该反应中被氧化的元素是________(填元素符号)。当该反应转移2.75 mol电子时,生成的二氧化硫在标准状况下的体积为________ L。
8SO2+2Fe2O3,该反应中被氧化的元素是________(填元素符号)。当该反应转移2.75 mol电子时,生成的二氧化硫在标准状况下的体积为________ L。
(2)实验室中用下列装置测定SO2催化氧化为SO3的转化率。(已知SO3的熔点为16.8 ℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响)

①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作:________________________________________。
②实验过程中,需要通入氧气。试写出一个用如下图所示装置制取氧气的化学方程式:________________________________________________________________________。

③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是________________________________________________________________________。
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是________(用含字母的代数式表示,不用化简)。
(3)某学习小组设计用如图装置验证二氧化硫的化学性质。

①能说明二氧化硫具有氧化性的实验现象为_________________________________。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验。
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀
上述方案中合理的是________(填“Ⅰ”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
离子晶体熔点的高低取决于晶体中晶格能的大小。判断KCl、NaCl、CaO、BaO四种晶体熔点的高低顺序是 ( )
A.KCl>NaCl>BaO>CaO
B.NaCl>KCl>CaO>BaO
C.CaO>BaO>NaCl>KCl
D.CaO>BaO>KCl>NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
Z基态原子的M层与K层电子数相等,它与某元素形成的化合物的晶胞如下图所示,晶胞中阴离子和阳离子的个数之比是___________________________。
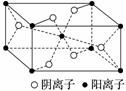
查看答案和解析>>
科目:高中化学 来源: 题型:
右图是金刚石晶体的结构示意图,则关于金刚石的描述不正确的是( )
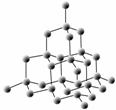
A.C—C键键角都为109.5°
B.最小的环由6个C原子构成
C.可溶于非极性溶剂
D.1 mol金刚石含有2 mol C—C键
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)氯酸钾熔化,粒子间克服了________的作用力;二氧化硅熔化,粒子间克服了________的作用力;碘的升华,粒子间克服了________的作用力。三种晶体的熔点由高到低的顺序是____________(填化学式)。
(2)下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,它们的熔点从低到高的顺序为________(填序号)。
(3)在H2、(NH4)2SO4、SiC、CO2、HF中,由极性键形成的非极性分子是________,由非极性键形成的非极性分子是________,能形成分子晶体的物质是________,含有氢键的晶体的化学式是________________________,属于离子晶体的是____________________,属于原子晶体的是____________________,五种物质的熔点由高到低的顺序是________________。
(4)A、B、C、D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3 500℃
试推断它们的晶体类型:
A.________________;B.________________;
C.________________;D.________________。
(5)相同压强下,部分元素氟化物的熔点见下表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/℃ | 1 266 | 1 534 | 183 |
试解释上表中氟化物熔点差异的原因:_____________________________________。
(6)镍粉在CO中低温加热,生成无色挥发性液态Ni(CO)4,呈四面体构型。150 ℃时,Ni(CO)4分解为Ni和CO。Ni(CO)是________晶体,Ni(CO)4易溶于下列________(填序号)
a.水 b.四氯化碳 c.苯 d.硫酸镍溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
具有广泛用途的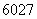 Co放射源首次实现了国内批量生产。另外,钴还有多种原子,如
Co放射源首次实现了国内批量生产。另外,钴还有多种原子,如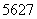 Co、
Co、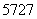 Co、
Co、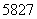 Co和
Co和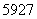 Co。下列关于钴原子的说法正确的是( )
Co。下列关于钴原子的说法正确的是( )
A.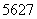 Co、
Co、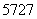 Co、
Co、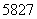 Co、
Co、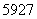 Co和
Co和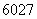 Co是摩尔质量不同的五种同素异形体
Co是摩尔质量不同的五种同素异形体
B.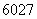 Co放射源可以用来治疗癌症,其中子数与电子数之差等于6
Co放射源可以用来治疗癌症,其中子数与电子数之差等于6
C.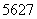 Co、
Co、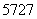 Co、
Co、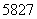 Co、
Co、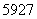 Co和
Co和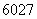 Co互为同位素,物理性质几乎相同,化学性质不同
Co互为同位素,物理性质几乎相同,化学性质不同
D.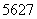 Co、
Co、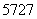 Co、
Co、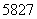 Co、
Co、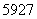 Co和
Co和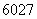 Co互为同分异构体
Co互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素的一个原子形成的离子可表示为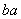 Xn-,下列说法正确的是 ( )
Xn-,下列说法正确的是 ( )
A.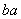 Xn-含有的中子数为a+b
Xn-含有的中子数为a+b
B.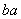 Xn-含有的电子数为a-n
Xn-含有的电子数为a-n
C.X原子的质量数为a+b+n
D.1个X原子的质量约为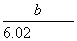 g
g
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中需要22.4 L(标准状况)SO2气体。化学小组同学依据化学方程式Zn+2H2SO4(浓)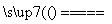 ZnSO4+SO2↑+2H2O计算后,取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g·cm-3)110 mL充分反应,锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
ZnSO4+SO2↑+2H2O计算后,取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g·cm-3)110 mL充分反应,锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
(1)化学小组所制得的气体中混有的主要杂质气体可能是______(填分子式)。产生这种结果的主要原因是________(用化学方程式和必要的文字加以说明)。
(2)为证实相关分析,化学小组的同学设计了实验,组装了如下装置,对所制取的气体进行探究。
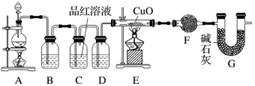
①装置B中加入的试剂为________,作用是________。
②装置D加入的试剂为________________,装置F加入的试剂为________________。
③可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有某杂质气体的实验现象是________。
④U形管G的作用为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com