
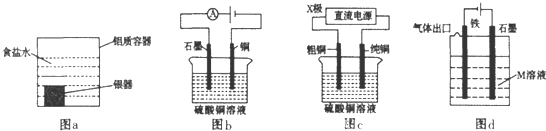
| A、利用图a装置处理银器表面的黑斑Ag2S,银器表面发生的反应为Ag2S+2e-=2Ag+S2- |
| B、图b电解一段时间,铜电极溶解,石墨电极上有亮红色物质析出 |
| C、图c中的X极若为负极,则该装置可实现粗铜的精炼 |
| D、图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| 选项 | 操作 | 现象 | 结论 |
| A | 常温下将Cu片放入浓H2SO4中 | 生成刺激性气味气体 | Cu与浓H2SO4反应生成SO2 |
| B | Al2(SO4)3溶液中滴加过量氨水 | 生成白色胶状物质 | Al(OH)3不溶于氨水 |
| C | 向某溶液中加入KSCN溶液,再向溶液中加入新制氯水 | 溶液先不显红色,加入氯水后变红色 | 该溶液中含有Fe2+ |
| D | 向某溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 该溶液中存在I- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、78g苯含有碳碳双键的数目为3NA |
| B、常温常压下,22.4L二氧化碳含有的原子总数为3NA |
| C、1mol Fe与足量稀HNO3反应,转移3NA个电子 |
| D、1L 1mol?L-1的NaClO溶液中含有ClO-的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
 铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中已铝为阳极,置于硫酸溶液中电解,装置如图,下列说法正确的是( )
铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中已铝为阳极,置于硫酸溶液中电解,装置如图,下列说法正确的是( )| A、阳极电极方程式为Al-3e+6OH-=Al2O3+H2O |
| B、随着电解的进行,溶液的PH逐渐增大 |
| C、当阴极生成气体3.36L(标况)时,阳极增重2.4g |
| D、电解过程中H+移向Al电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 无机酸 | 氢氰酸(HCN) | 碳酸(H2CO3) | 氢氟酸(HF) |
| 电离平衡常数K值 | 6.2×10-10(K) | 4.2×10-7(K1) 5.6×10-11(K2) |
6.61×10-4(K) |
| A、氟化钠溶液中通入过量CO2 F-+H2O+CO2=HF+HCO3- |
| B、Na2CO3溶液中2C(Na+)=C(CO32-)+C(HCO3-)+C(H2CO3) |
| C、中和等体积、等pH的氢氰酸(HCN)和氢氟酸(HF)消耗NaOH的量前者大于后者 |
| D、等浓度的NaCN和NaF溶液中PH值前者小于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++H++OH-+SO42-═BaSO4↓+H2O | ||||
B、向铜作电极电解硫酸溶液:2H2O
| ||||
| C、向NaClO溶液中通入过量SO2:ClO-+SO2+H2O═HClO+HSO3- | ||||
| D、向AlCl3溶液中加入过量的Na:Al3++4Na+2H2O═AlO2-+4Na++2H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素A在周期表中的位置为第2周期ⅥA族 |
| B、元素A、B、C的原子半径由大到小的顺序为r(C)>r(B)>r(A) |
| C、A、B两种元素的氢化物的稳定性A>B |
| D、1mol C2B2与足量的AB2完全反应转移约6.02×1023个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com