
| A、常温下将等体积等物质的量浓度的醋酸钠与盐酸两溶液混合:c(Na+)>c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) |
| B、向NH4HSO4溶液中滴加含等物质的量溶质的NaOH溶液:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| C、在0.1mol/L(NH4)2Fe(SO4)2溶液中:c(H+)+c(NH4+)+2c(Fe2+)=c(OH-)+c(SO42-) |
| D、pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |


科目:高中化学 来源: 题型:
| A、C3H6和C4H6O2 |
| B、C2H4和C2H6O |
| C、C2H2和C6H6 |
| D、CH4O和C3H4O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
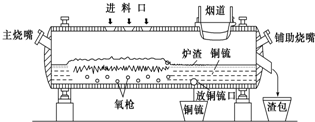 高富氧底吹熔池炼铜新工艺反应炉如图
高富氧底吹熔池炼铜新工艺反应炉如图查看答案和解析>>
科目:高中化学 来源: 题型:
| A、糖类是人体获得能量的唯一来源 |
| B、没有蛋白质就没有生命 |
| C、油脂在人体内酶的作用下,可重新合成人体所需的脂肪等物质 |
| D、人体所需的菅养素主要有糖类、油脂、蛋白质、无机盐、维生素和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 电解原理在化学工业中有广泛应用.如图中甲、乙为相互串联的两电解池.请回答:
电解原理在化学工业中有广泛应用.如图中甲、乙为相互串联的两电解池.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| 15 |
| 16 |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com