
| A. | 金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 | |
| B. | 在NaCl晶体中每个Na+(或Cl-)周围都紧邻6个Cl-(或6个Na+) | |
| C. | 白磷晶体中,粒子之间通过共价键结合,键角为60° | |
| D. | 离子晶体在熔化时,离子键被破坏;而分子晶体熔化时,化学键不被破坏 |
分析 A.金刚石晶体中,每个碳原子形成四个共价键,由共价键形成的最小碳环上有6个碳原子;
B.氯化钠晶体中钠离子或氯离子的配位数都是6;
C.白磷分子为正四面体结构,原子间通过共价键结合,键角为60°;
D.离子晶体的构成微粒是阴阳离子,分子晶体的构成微粒是分子.
解答 解:A.金刚石晶体中,由共价键形成的最小碳环上有6个碳原子,每个碳原子形成四个共价键,从而形成空间网状结构,故A正确;
B.氯化钠晶体中钠离子或氯离子的配位数都是6,所以在NaCl晶体中每个Na+(或C1-)周围都紧邻6个Cl-(或Na+),故B正确;
C.白磷分子为正四面体结构,原子间通过共价键结合,键角为60°,分子间存在范德华力,故C错误;
D.离子晶体的构成微粒是阴阳离子,分子晶体的构成微粒是分子,所以离子晶体在熔融状态下能电离出阴阳离子,而分子晶体在熔融状态下还是以分子存在,只破坏分子间作用力不破坏化学键,故D正确;
故选C.
点评 本题考查了晶体的有关知识,明确晶体结构是解本题关键,熟练掌握教材中各种晶体代表物的结构特点,灵活运用这些知识点分析解答问题,易错选项是B,注意B选项题干中是“微粒间”而不是“原子间”,导致很多粗心同学易错,解答时仔细审题,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | HF的电子式: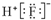 | |
| B. | 二氧化碳的结构式:O=C=O | |
| C. | Cl-离子的结构示意图: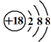 | |
| D. | 质子数为6,中子数为8的微粒:${\;}_{6}^{8}$C |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使溴的四氯化碳溶液褪色 | |
| B. | 将苯滴入溴水中,振荡后水层接近无色 | |
| C. | 乙烯使酸性高锰酸钾溶液褪色 | |
| D. | 甲烷与氯气混合,光照一段时间后黄绿色消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
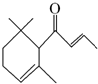 一种从植物中提取的天然化合物αdamascone可用于制作“香水”,其结构为:有关该化合物的下列说法不正确的是( )
一种从植物中提取的天然化合物αdamascone可用于制作“香水”,其结构为:有关该化合物的下列说法不正确的是( )| A. | 分子式为C13H20O | |
| B. | 该化合物可发生聚合反应 | |
| C. | 1 mol该化合物完全燃烧消耗19 mol O2 | |
| D. | 与足量溴水加成,最多消耗Br22 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
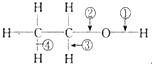 下列关于乙醇在各种不同反应中断裂键的说明中,正确的是( )
下列关于乙醇在各种不同反应中断裂键的说明中,正确的是( )| A. | 和金属钠反应,键③断裂 | B. | 和金属钠反应,键②断裂 | ||
| C. | 在Cu催化下和O2反应,键①、③断裂 | D. | 在Cu催化下和O2反应,键②、③断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
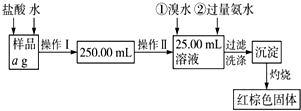 某氯化铁样品含有少量FeCl2杂质.现要测定其中铁元素的质量分数,实验按以下步骤进行:请根据流程,回答以下问题:
某氯化铁样品含有少量FeCl2杂质.现要测定其中铁元素的质量分数,实验按以下步骤进行:请根据流程,回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Fe(SCN)3溶液中加入固体KSCN后颜色变深 | |
| B. | 棕红色NO2加压后颜色先变深后变浅 | |
| C. | SO2催化氧化成SO3的反应,往往需要使用催化剂 | |
| D. | H2、I2、HI平衡混合气加压后颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用浸泡过高锰酸钾溶液的硅藻土吸收水果产生的乙烯以达到保鲜的要求 | |
| B. | 世博会期间,利用可降解的“玉米塑料”替代常用的一次性饭盒,可防止产生白色污染 | |
| C. | 蛋白质、淀粉、纤维素这些生活中的常见物质都是天然高分子化合物 | |
| D. | 煤经气化和液化两个物理过程,可变为清洁能源 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com