
| 实验内容 | 实验目的 | |
| A | 向某未知溶液中加人BaCl2溶液后,再加人稀硝酸观察沉淀的生成 | 检验是否含 SO42-离子 |
| B | 向某未知溶液中加人NaOH固体,加热,在管口用湿润的蓝色石蕊试纸检验 | 检验是否含NH4+离子 |
| C | 加热分别用SO2和HClO漂白后的品红溶液 | 探究SO2和HCIO漂白原理的不同 |
| D | 加热盛有浓硫酸和铜的试管 | 探究浓硫酸的脱水性 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.能和氯化钡反应且生成不溶于稀硝酸的离子还有银离子等,且硝酸具有强氧化性;
B.应用红色石蕊试纸;
C.次氯酸的漂白性具有永久性、二氧化硫的漂白性具有暂时性;
D.用浓硫酸和蔗糖探究浓硫酸的脱水性.
解答 解:A.能和氯化钡反应且生成不溶于稀硝酸的离子还有银离子等,且硝酸具有强氧化性,向某未知溶液中加入BaCl2溶液后,再加入稀硝酸观察沉淀的生成,生成的沉淀可能是硫酸钡或氯化银,且硝酸能将亚硫酸根离子或亚硫酸氢根离子氧化生成硫酸根离子,所以不能据此判断含有SO42-,故A错误;
B.氨水溶液呈碱性,可使红色石蕊试纸变蓝,应用红色石蕊试纸,故B错误;
C.次氯酸的漂白性具有永久性、二氧化硫的漂白性具有暂时性,所以可以用加热分别用SO2和HClO漂白后的品红溶液的方法探究SO2和HClO漂白原理的不同,故C正确;
D.用浓硫酸和蔗糖探究浓硫酸的脱水性,浓硫酸和铜的反应体现浓硫酸的强氧化性和酸性,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及物质性质及其检验、离子检验等知识点,侧重考查学生分析判断及探究能力,明确物质性质是解本题关键,易错选项是B,试题培养了学生的化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | 15g甲基(-CH3)所含有的电子数是10 NA个 | |
| B. | 标准状况下,2.24 L CHCl3的原子总数为0.5 NA个 | |
| C. | 4.2g C3H6中含有的碳碳双键数一定为0.1NA | |
| D. | 常温下,14g乙烯和丙烯的混合物中总原子数为3NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
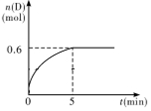
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.57 mol | B. | 2.25mol | C. | 2 mol | D. | 0.63mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 含氯消毒剂和过氧化物等强氧化性消毒剂可防甲型H1N1流感.
含氯消毒剂和过氧化物等强氧化性消毒剂可防甲型H1N1流感.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 钠与硫酸铜溶液的反应:2Na+Cu2+═2Na++Cu | |
| C. | 铁与稀盐酸的反应:2Fe+6H+═2 Fe 3++3H2↑ | |
| D. | 铝粉和氢氧化钠溶液的反应:2Al+2 OH-═2AlO2-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com