
【题目】测定稀硫酸和氢氧化钠溶液反应的中和热(实验装置如下图所示)。
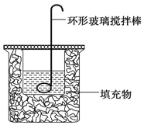
(1)图中尚缺少的一种仪器是__________
(2)烧杯间填满碎纸屑的作用是__________。
(3)写出反应的热化学方程_____________________(中和热为57.3kJ·mol-1)。
(4)该同学每次分别取0.50mol·L-1 50mL NaOH溶液和0.50mol·L-1 30mL硫酸进行实验,通过多次实验测定中和热ΔH=-53.5kJ·mol-1,与57.3kJ·mol-1有偏差,产生偏差的原因不可能是__________(填字母)。
a.实验装置保温、隔热效果差
b.用量筒量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度
(5)在测定中和热的实验中,下列说法正确的是(____________)
A.使用环形玻璃棒是为了加快反应速率,减小实验误差
B.为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触
C.用0.5mol·L-1 NaOH溶液分别与0.5mol·L-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同
D.在测定中和热实验中需要使用的仪器有天平、量筒、烧杯、滴定管、温度计
(6)用相同浓度和体积的氨水代替溶液进行上述实验,测得的中和热的数值会__________;(填“偏大”、“偏小”或“无影响”)。
(7))你认为CH3COOH的中和热与HCl的中和热数值相比,________较大,其原因是______________________________________________________。
(8)若三次平行操作测得数据中起始时盐酸与烧碱溶液平均温度相同,而终止温度与起始温度差t2-t1分别为①2.2 ℃ ②2.4 ℃ ③3.4 ℃,则最终代入计算式的温差均值为________ ℃。
【答案】温度计 保温隔热,减少实验过程中热量的损失 H+(aq)+OH-(aq)![]() H2O(l) ΔH=-57.3kJ/mol b A 偏小 HCl CH3COOH是弱酸,只少部分电离,发生电离时要吸热 2.3
H2O(l) ΔH=-57.3kJ/mol b A 偏小 HCl CH3COOH是弱酸,只少部分电离,发生电离时要吸热 2.3
【解析】
测定中和反应的反应热时,利用的原理是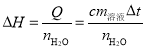 ;使用的试剂是稀的强酸碱,如稀NaOH溶液和稀硫酸,为了保证反应彻底,某一种要稍微过量;由于要测混合溶液反应前后的温度变化,所以实验装置一定要注意保温;在烧杯之间填充碎纸屑,使用环形玻璃搅拌棒而不用金属搅拌棒等都是为了保温,减少热量的散失;为了数据的准确性,一般需要多次测量,通过求温度变化的平均值来更准确地计算中和热。
;使用的试剂是稀的强酸碱,如稀NaOH溶液和稀硫酸,为了保证反应彻底,某一种要稍微过量;由于要测混合溶液反应前后的温度变化,所以实验装置一定要注意保温;在烧杯之间填充碎纸屑,使用环形玻璃搅拌棒而不用金属搅拌棒等都是为了保温,减少热量的散失;为了数据的准确性,一般需要多次测量,通过求温度变化的平均值来更准确地计算中和热。
(1)为了测定反应前后溶液温度的变化,需要用到温度计;
(2)烧杯之间填充碎纸屑,是为了保温隔热,减少热量的散失,从而提高实验的准确性;
(3)中和反应的热化学方程式为:![]()
![]() ;
;
(4)a.实验装置若保温措施不到位,则测得的中和反应放出的热量会偏少,那么最终计算得到的![]() 绝对值偏小,a项可能;
绝对值偏小,a项可能;
b.由于NaOH和H2SO4浓度相同,所以30mL的硫酸相对于50mL的NaOH溶液而言是过量的;在用量筒量取50mLNaOH溶液时,若仰视会导致量取的NaOH偏多;因此中和时会放出更多的热量,进而导致计算的![]() 绝对值偏大,b项不可能;
绝对值偏大,b项不可能;
c.在向烧杯中加入NaOH溶液时,若分多次进行,那么由于热量的散失,会导致记录的温度的变化值比正常值偏低,由此计算的中和反应放出的热量偏少,那么最终计算的![]() 绝对值偏小,c项可能;
绝对值偏小,c项可能;
d.温度计在测完NaOH溶液的温度后,一定要用水冲洗去表面残留的NaOH溶液后再去测量硫酸的温度;若不进行冲洗直接测量,则由于温度计表面残留的NaOH与硫酸反应放热而导致记录的初始温度偏大,进而导致计算的![]() 偏小,那么计算所得的中和反应放出的热量就偏少,由此计算的
偏小,那么计算所得的中和反应放出的热量就偏少,由此计算的![]() 绝对值偏小,d项可能;
绝对值偏小,d项可能;
答案选b;
(5)A.使用环形玻璃搅拌棒搅拌混合后的溶液,让二者反应更快更充分,这样可以减少误差,A项正确;
B.温度计测量的是溶液的温度,不能使其与容器壁接触,B项错误;
C.由于醋酸是弱酸,弱酸的解离过程会吸收热量,因此由其测得的中和热数值与由盐酸测得的不同,C项错误;
D.中和反应反应热的测定实验中不需要用到滴定管,D项错误;
答案选A;
(6)![]() 是弱电解质,弱电解质电离时会吸收热量,因此会导致测得的中和反应放出的热量偏小,由此计算所得的中和热的数值偏小;
是弱电解质,弱电解质电离时会吸收热量,因此会导致测得的中和反应放出的热量偏小,由此计算所得的中和热的数值偏小;
(7)醋酸是弱酸,发生电离时要吸收热量,因此导致醋酸的中和热的数值更小;
(8)由题可知,温度差3.4℃偏离均值过大,所以判定为无效数据,计算平均值时应当在2.2℃和2.4℃之间进行计算,因此代入计算式的温差均值为2.3℃。


 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:
【题目】关于下列各实验装置的叙述中,不正确的是( )
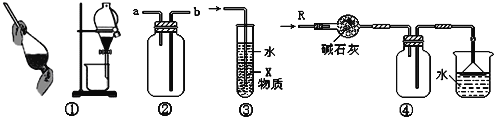
A. 装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体
B. 装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸
C. 装置①可用于分离C2H5OH和H2O的混合物
D. 装置④可用于干燥、收集NH3,并吸收多余的NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)烷烃A的碳原子数是5,则符合A的结构有____________ 种,其中含有四个甲基的系统命名为________________________________ ;
(2)烷烃B在同温同压下蒸气的密度是H2的43倍,则B的分子式为____________,其中含有3个-CH3的同分异构体的结构简式为___________________________、________________________________;
(3)某气态烃在标准状况下的密度为2.59g/L,该烃的含碳量为82.8%,则分子中碳、氢原子的个数比是______________,分子式是_________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①H2(g)+![]() O2(g)=H2O(g) ΔH1=-241.8kJ·mol-1;
O2(g)=H2O(g) ΔH1=-241.8kJ·mol-1;
②H2(g)+![]() O2(g)=H2O(l) ΔH2=-285.8kJ·mol-1。
O2(g)=H2O(l) ΔH2=-285.8kJ·mol-1。
气态分子中的化学键 | 断开1mol化学键所需的能量/kJ |
O—H | 465 |
O=O | 498 |
下列说法不正确的是( )
A.氢气的燃烧热ΔH=-241.8kJ·mol-1
B.断开1molH—H键需要吸收439.2kJ的能量
C.相同条件下,1molH2O(g)比1molH2O(l)能量高
D.18gH2O(l)完全分解生成氢气和氧气,需要吸收285.8kJ的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2的结构可以表示为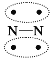 ,CO的结构可以表示为
,CO的结构可以表示为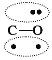 ,其中椭圆框表示 π键,下列说法不正确的是( )
,其中椭圆框表示 π键,下列说法不正确的是( )
A.N2 分子与 CO 分子中都含有三键
B.CO 分子中有一个 π 键是配位键
C.N2 与 CO 互为等电子体
D.N2 与 CO 的化学性质相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在已经发现的一百多种元素中,除稀有气体外,非金属元素只有十多种,但与生产生活有密切的联系。
(1)短周期中可以做半导体材料的元素的最高价氧化物与烧碱溶液反应的离子方程式是:__________;
(2)为了提高煤的利用率,常将其气化或液化,其中一种液化是将气化得到的氢气和一氧化碳在催化剂作用下转化为甲醇,写出该化学反应方程式为____________;
(3)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
①合成氨的反应中的能量变化如图所示。该反应是________反应(填“吸热”或“放热”)。
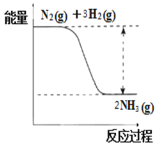
②在一定条件下,将2.5mol N2和7.5mol H2的混合气体充入体积为2L的固定闭容器中发生反应:N2(g)+ 3H2(g) ![]() 2NH3(g),5分钟末时达到平衡,测得容器内的压强是开始时的0.9倍,则5分钟内用氨气表示该反应的平均化学反应速率为:V(NH3)=____________;氢气达到平衡时的转化率是_____________(保留小数点后一位);
2NH3(g),5分钟末时达到平衡,测得容器内的压强是开始时的0.9倍,则5分钟内用氨气表示该反应的平均化学反应速率为:V(NH3)=____________;氢气达到平衡时的转化率是_____________(保留小数点后一位);
(4)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示:
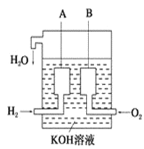
A,B两个电极均由多孔的碳块组成。该电池的正极反应式为:________________;若将上述装置中的氢气换成甲烷,其余都不改变,对应装置的负极反应方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇是重要的有机化工原料,可由乙烯水合法生产,反应的化学方程式如下:C2H4(g)+ H2O(g)![]() C2H5OH(g),下图为乙烯的平衡转化率与温度(T)、压强(P)的关系[起始n(C2H4)∶n(H2O) =1∶1]。下列有关叙述正确的是
C2H5OH(g),下图为乙烯的平衡转化率与温度(T)、压强(P)的关系[起始n(C2H4)∶n(H2O) =1∶1]。下列有关叙述正确的是

A. Y对应的乙醇的质量分数为1/9
B. X、Y、Z对应的反应速率:υ(X) > υ(Y) > υ(Z)
C. X、Y、Z对应的平衡常数数值:KX > KY > KZ
D. 增大压强、升高温度均可提高乙烯的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在探究新制氯水成分及性质的实验中,依据下列方法和现象,不能得出相应结论的是( )
选项 | 方法 | 现象 | 结论 |
A | 观察氯水颜色 | 氯水呈黄绿色 | 氯水中含Cl2 |
B | 向饱和NaHCO3溶液中加入足量氯水 | 有无色气体产生 | 氯水中含HClO |
C | 向红色纸条上滴加氯水 | 红色纸条褪色 | 氯水具有漂白性 |
D | 向FeCl2溶液中滴加氯水 | 溶液变成棕黄色 | 氯水具有氧化性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、生产、环境等密切相关。下列说法错误的是
A.煤的液化、石油的裂化和油脂的皂化都属于化学变化
B.棉、丝、毛、油脂都是天然有机高分子化合物
C.乙烯与氧气在银催化作用下生成环氧乙烷原子利用率为100%
D.海水淡化的方法有蒸馏法、电渗析法等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com