
| A£® | Ö»ÓŠ¢Ł¢Ś | B£® | Ö»ÓŠ¢Ś¢Ū¢Ż | C£® | Č«²æ | D£® | Ö»ÓŠ¢Ū |
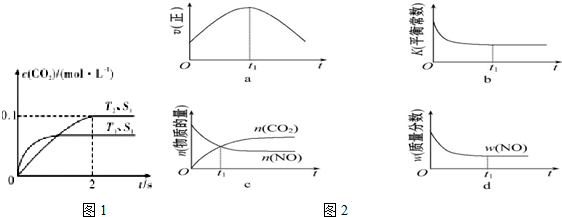
·ÖĪö ¢Ł³ōŃõæÕ¶“Ö÷ŅŖÓė·śĀČ“śĢžµČ¹żĮæÅÅ·ÅŌģ³É£»
¢Ś¶žŃõ»ÆµŖµČµŖµÄŃõ»ÆĪļµÄÅÅ·ÅŹĒ¹ā»ÆѧŃĢĪķµÄÖ÷ŅŖŌŅņ£»
¢ŪÓźµÄÖ÷ŅŖŠĪ³ÉŌŅņŹĒŅņĪŖ¹ż¶ČŹ¹ÓĆŗ¬Įņ»ÆŹÆČ¼ĮĻ£¬SO2¹ż¶ČÅÅ·ÅŌģ³É£»
¢Ü¾ŪŅŅĻ©ĖÜĮĻ²»Äܽµ½ā£¬ŹĒ°×É«ĪŪČ¾µÄŌŅņ£»
¢Ż¶ņ¶ūÄįŵ”±ĻÖĻóŹĒÓÉæÕĘųÖŠCO2ÅضČŌö“óŅżĘšµÄ£»
¢ŽŌģ³ÉĪĀŹŅŠ§Ó¦µÄĘųĢåŹĒ¶žŃõ»ÆĢ¼£»
¢ß³±ŹĒŗ¬N”¢PŌŖĖŲµÄĪŪĖ®¹ż¶ČÅÅ·Å£¬Ōģ³ÉĖ®Ģåø»ÓŖŃų»Æ£®
½ā“š ½ā£ŗ¢Ł³ōŃõæÕ¶“ŹĒ·śĀČ“śĢžµČµÄ¹żĮæÅÅ·ÅŌģ³É£¬¹ŹÕżČ·£»
¢Ś”°¹ā»ÆѧŃĢĪķ”±Ö÷ŅŖŹĒÓÉNO2µČŅżĘšµÄ£¬¹ŹÕżČ·£»
¢ŪĖįÓźµÄÖ÷ŅŖŠĪ³ÉŌŅņŹĒŅņĪŖ¹ż¶ČŹ¹ÓĆŗ¬Įņ»ÆŹÆČ¼ĮĻ£¬SO2¹ż¶ČÅÅ·ÅŌģ³É£¬¹Ź“ķĪó£»
¢Ü”¢”°°×É«ĪŪČ¾”±Ö÷ŅŖŹĒÓɾŪŅŅĻ©ĖÜĮĻµČŅżĘšµÄ£¬¹ŹÕżČ·£»
¢Ż¶ņ¶ūÄįŵ”±ĻÖĻóŹĒÓÉæÕĘųÖŠCO2ÅضČŌö“óŅżĘšµÄ£¬¹ŹÕżČ·£»
¢Ž”°ĪĀŹŅŠ§Ó¦”±Ö÷ŅŖŹĒÓÉæÕĘųÖŠCO2ÅضČŌö“óŅżĘšµÄ£¬¹ŹÕżČ·£»
¢ß”°³ą³±”±Ö÷ŅŖŹĒÓÉĖ®ĢåÖŠP”¢NµČŌŖĖŲ¹żĮæŅżĘšµÄ£¬Ōģ³ÉĖ®Ģåø»ÓŖŃų»Æ£¬¹ŹÕżČ·£»
¹ŹŃ”£ŗD£®
µćĘĄ ±¾Ģāæ¼²éĮĖÉś»īÖŠµÄ»Æѧ£¬ŹģĻ¤Éś»īÖŠ³£¼ūµÄ»·¾³ĪŪČ¾ÓėÖĪĄķŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŠÅĻ¢Ņ»£ŗøõĶ¬Äų”¢īÜ”¢ĢśµČ½šŹōæÉŅŌ¹¹³ÉøßĪĀŗĻ½š”¢µēČČŗĻ½š”¢¾«ĆÜŗĻ½šµČ£¬ÓĆÓŚŗ½æÕ”¢Óīŗ½”¢µēĘ÷¼°ŅĒ±ķµČ¹¤Ņµ²æĆÅ£®
ŠÅĻ¢Ņ»£ŗøõĶ¬Äų”¢īÜ”¢ĢśµČ½šŹōæÉŅŌ¹¹³ÉøßĪĀŗĻ½š”¢µēČČŗĻ½š”¢¾«ĆÜŗĻ½šµČ£¬ÓĆÓŚŗ½æÕ”¢Óīŗ½”¢µēĘ÷¼°ŅĒ±ķµČ¹¤Ņµ²æĆÅ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
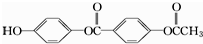
| A£® | 3 mol | B£® | 4mol | C£® | 5 mol | D£® | 6 mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
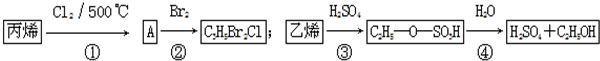
| A£® | ·“Ó¦¢ŁÓė·“Ó¦¢Ü¾łŹĒČ”“ś·“Ó¦ | |
| B£® | ·“Ó¦¢ŚÓė·“Ó¦¢Ū¾łŹĒ¼Ó³É·“Ó¦ | |
| C£® | ·“Ó¦¢ŚÖŠ²śĪļµÄ½į¹¹¼ņŹ½ĪŖCH2BrCH2CHClBr | |
| D£® | ·“Ó¦¢Ū”¢¢Ü±ķĆ÷ĮņĖįŹĒŅŅĻ©ÓėĖ®·“Ó¦µÄ“߻ƼĮ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3£ŗ2£ŗ1 | B£® | 1£ŗ2£ŗ3 | C£® | 3£ŗ1£ŗ1 | D£® | 1£ŗ3£ŗ3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÅäÖĆĮņĖįČÜŅŗŹ±£¬½«ÅØĮņĖįĀżĀż×¢ČėŹ¢ÓŠĖ®µÄČŻĮæĘæÖŠ½ųŠŠÅäÖĘ | |
| B£® | ÓĆĶŠÅĢĢģĘ½³ĘĮæ8.75g NaCl¹ĢĢå | |
| C£® | ½«»ģŗĻŅŗÕōĮó·ÖĄėŹ±£¬Ó¦Ź¹ĪĀ¶Č¼ĘĖ®ŅųĒņ½žĆ»ŌŚ»ģŗĻŅŗÖŠ | |
| D£® | ·ÖŅŗŹ±£¬½«ÉĻ²ćŅŗĢå“Ó·ÖŅŗĀ©¶·ÉĻæŚµ¹³ö£¬ĻĀ²ćŅŗĢå“Ó·ÖŅŗĀ©¶·ĻĀæŚ·Å³ö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 4ÖÖ | B£® | 5ÖÖ | C£® | 6ÖÖ | D£® | 7ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com