
| A. | 反应Ⅰ中SO2是还原剂 | B. | 反应Ⅲ中H2是还原产物 | ||
| C. | 氧化性强弱顺序:H2SO4>I2>SO2 | D. | 该转化关系可实现分解H2O制取H2 |
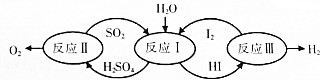
分析 A.根据图知,反应I中发生的反应为I2+SO2+2H2O=2HI+H2SO4,该反应中S元素化合价由+4价变为+6价、I元素化合价由0价变为-1价,失电子的反应物的还原剂;
B.反应III中反应方程式为2HI=I2+H2,该反应中碘是氧化产物、氢气是还原产物;
C.同一氧化还原反应中氧化性强弱顺序:氧化剂>氧化产物;
D.根据图知,碘和二氧化硫能循环利用,实质上是水分解生成氢气和氧气.
解答 解:A.根据图知,反应I中发生的反应为I2+SO2+2H2O=2HI+H2SO4,该反应中S元素化合价由+4价变为+6价、I元素化合价由0价变为-1价,失电子的反应物的还原剂,所以反应Ⅰ中SO2是还原剂,故A正确;
B.反应III中反应方程式为2HI=I2+H2,氧化剂对应的产物是还原产物、还原剂对应的产物是氧化产物,所以该反应中碘是氧化产物、氢气是还原产物,故B正确;
C.同一氧化还原反应中氧化性强弱顺序:氧化剂>氧化产物,根据I2+SO2+2H2O=2HI+H2SO4知,氧化性H2SO4<I2,故C错误;
D.根据图知,碘和二氧化硫能循环利用,实质上是水分解生成氢气和氧气,所以该转化关系可实现分解H2O制取H2,故D正确;
故选C.
点评 本题考查氧化还原反应,为高频考点,侧重考查基本概念,明确氧化剂、还原剂、氧化产物和还原产物概念及氧化性强弱比较方法是解本题关键,会正确书写相应的化学方程式,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 滴定前,没有逐出滴定管下口的气泡 | |
| B. | 用甲基橙作指示剂,指示剂刚变色,就停止滴定 | |
| C. | 酸式滴定管用蒸馏水洗净后,直接加入己知浓度的盐酸 | |
| D. | 锥形瓶用蒸馏水洗净后,直接加入一定体积的未知浓度的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe→FeSO4 | B. | NaOH→NaCl | C. | CaO→CaSO4 | D. | CaCO3→CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向溶液中加入稀盐酸可以促进氨水的电离,溶液的碱性增强 | |
| B. | 向溶液中加入等体积的pH=2盐酸后溶液呈酸性 | |
| C. | 由水电离产生的c(OH-)=10-12mol•L-1 | |
| D. | 向溶液中加入适量盐酸使混合液的pH=7,混合液中c(NH4+)>c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
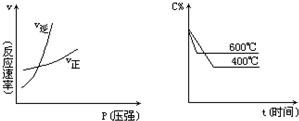
| A. | 吸热反应,m+n<p | B. | 吸热反应,m+n>p | C. | 放热反应,m+n<p | D. | 放热反应,m+n>p |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
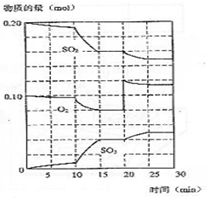 在一定条件下发生如下反应:2SO2(g)+O2 (g)?2SO3(g);△H<0
在一定条件下发生如下反应:2SO2(g)+O2 (g)?2SO3(g);△H<0查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡常数减小 | B. | CaO的量减少 | C. | 氧气浓度变大 | D. | CaO2的量不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com