
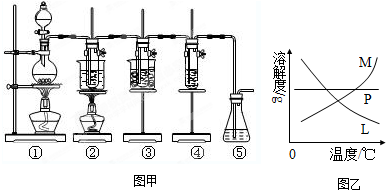
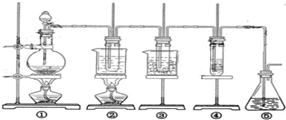
如图所示,比较不同浓度的硫代硫酸钠溶液和同浓度的硫酸反应的速率大小的实验中,锥形瓶瓶底衬有画了“十”字的白纸,先向瓶内加入硫代硫酸钠溶液,再加入硫酸溶液。需记录反应所需的时间,正确的记时方法是

A.加入硫代硫酸钠溶液后即开始记时,瓶中出现浑浊现象时记时结束
B.加入硫代硫酸钠溶液后即开始记时,加入硫酸溶液后记时结束
C.加入硫酸溶液后即开始记时,瓶中出现浑浊现象记时结束
D.加入硫酸溶液后即开始记时,至看不到瓶底“十”字记时结束
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
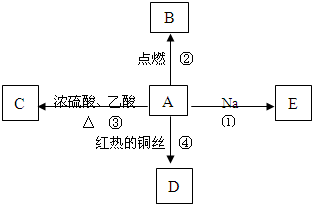 A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
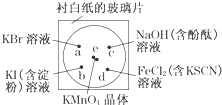 化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求.某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好.[已知:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O]
化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求.某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好.[已知:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O]查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
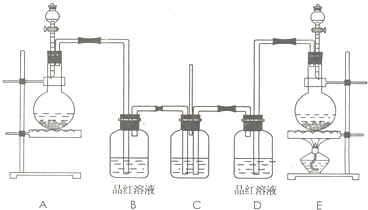
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为 红 红 色 |
氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成的HClO将石蕊氧化为无色物质 氯气与水反应生成的HClO将石蕊氧化为无色物质 |
| 然后溶液从无色逐渐变为 黄绿 黄绿 色 |
继续通入的氯气溶于水使溶液呈黄绿色 继续通入的氯气溶于水使溶液呈黄绿色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com