
| A、稀硫酸滴在银片上:Ag+2H+=Ag++H2↑ |
| B、硫酸镁溶液与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
| C、硝酸银溶液与盐酸反应:Ag++Cl-=AgCl↓ |
| D、澄清石灰水与碳酸钠溶液反应:Ca(OH)2+CO32-=CaCO3↓+H2O |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、配制1mol?L-1NaOH溶液时,将溶解后的NaOH溶液立即注入容量瓶 | ||
| B、用小刀切下一小块金属钠,将剩余的钠再放回原试剂瓶 | ||
C、向某溶液中加入BaCl2溶液产生白色沉淀,再加稀盐酸沉淀不溶解,说明原溶液中一定含有S
| ||
| D、向沸水中逐滴滴加1mol?L-1FeCl3溶液,并不断用玻璃棒搅拌,可制得Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、区别晶体与非晶体最可靠的科学方法是对固体进行x-射线衍射实验 |
| B、非晶体中粒子的排列无序,所以非晶体具有各向异性 |
| C、晶体有自范性 |
| D、非晶体无固定熔点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
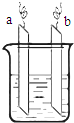 图中,两电极上发生的电极反应分别为:a极:Ag++e-=Ag;b极:Fe-2e-=Fe2+下列说法不正确的是( )
图中,两电极上发生的电极反应分别为:a极:Ag++e-=Ag;b极:Fe-2e-=Fe2+下列说法不正确的是( )| A、a、b可能是同种电极材料 |
| B、该装置一定是电解池 |
| C、装置中电解质溶液一定含有Ag+ |
| D、装置中发生的反应方程式一定是Fe+2Ag+═Fe2++2Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同主族元素从上到下,单质的熔点逐渐降低 |
| B、同周期元素(除0族元素外)从左到右,原子半径逐渐减小 |
| C、第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强 |
| D、第IA族元素铯的两种同位素137Cs比133Cs多4个质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、①④ | C、②③ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
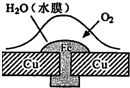
| A、铁铆钉在此环境下不易被腐蚀 |
| B、原电池反应的化学方程式:2Fe+O2+2H2O═2Fe(OH)2 |
| C、与铁接触的水膜发生反应:O2+4Fe-+2H2O═4OH- |
| D、如果在酸雨环境中,将发生:Cu-2e-═Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、K=
| ||
B、K=
| ||
| C、增大c(H2O)或减小c(H2),会使该反应平衡常数减小 | ||
| D、改变反应的温度,平衡常数不一定变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O和Na2O2组成元素相同,与CO2反应产物也相同 |
| B、SO2和CO2都是酸性氧化物,都能与NaOH溶液反应 |
| C、NO和NO2的密度均比空气大,都可用向上排空气法收集 |
| D、C3H8和CH3CH2OH相对分子质量相近,分子间作用力相近,二者沸点也相近 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com