
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
| A | B | C | ||
| (1) | 1 | 3 | 0 | 放出热量a kJ |
| (2) | 0 | 0 | 2 | 吸收热量b kJ |
| (3) | 2 | 6 | 0 | 放出热量c kJ |
| A. | A的体积分数:(2)>(1)>(3) | |
| B. | 三个容器内反应的平衡常数:K(3)=K2(1)=K2(2) | |
| C. | 达平衡时体系压强:P(3)=2P(1) | |
| D. | 热量关系:a+b=50 |
分析 A.(1)与(2)为完全等效平衡,平衡时相同物质的体积分数相等;
(1)中A、B按物质的量1:3反应,起始物质的量之比也是1:3,则平衡时A、B体积分数之比为1:3,(3)到达的平衡相当于在(1)的平衡基础上压强增大1倍,平衡向右移动,C的物质的量增大、混合气体总的物质的量减小,C的体积分数增大,则(3)中A、B总体积分数减小;
B.平衡常数只与温度有关,温度相同,平衡常数相同;
C.(3)与(1)相比,(3)到达的平衡相当于在(1)的平衡基础上压强增大1倍,平衡向右移动;
D.(2)与(1)相比,二者为完全等效平衡,平衡时相同组分的物质的量相等,设平衡时A的物质的量为nmol,再计算反应热判断.
解答 解:A.(1)与(2)为完全等效平衡,平衡时相同物质的体积分数相等,则A的体积分数:(2)=(1);(1)中A、B按物质的量1:3反应,起始物质的量之比也是1:3,则平衡时A、B体积分数之比为1:3,(3)到达的平衡相当于在(1)的平衡基础上压强增大1倍,平衡向右移动,C的物质的量增大、混合气体总的物质的量减小,C的体积分数增大,则(3)中A、B总体积分数减小,则A的体积分数:(1)>(3),故A的体积分数:(2)=(1)>(3),故A错误;
B.平衡常数只与温度有关,三容器内温度相同,平衡常数相同,即:K(3)=K(1)=K(2),故B错误,
C.(3)与(1)相比,(3)到达的平衡相当于在(1)的平衡基础上压强增大1倍,平衡向右移动,则P(3)<2P(1),故C错误;
D.(2)与(1)相比,二者为完全等效平衡,平衡时相同组分的物质的量相等,设平衡时A的物质的量为nmol,则a=(1-n)×50,b=50n,故a+b=(1-n)×50+50n=50,故D正确,
故选:D.
点评 本题考查化学平衡计算与影响因素,注意利用等效思想进行分析解答,关键是根据等效平衡建立的途径,难度中等.


科目:高中化学 来源: 题型:解答题
 ;镁条在气体B中燃烧生成的物质是Mg3N2(填化学式);
;镁条在气体B中燃烧生成的物质是Mg3N2(填化学式);查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小于50mL | B. | 等于50mL | C. | 大于50mL | D. | 等于50/ρmL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol NH4+所含有的电子数为11 NA | |
| B. | 20g氖气所含有的分子数约为 3.01×1023 | |
| C. | 标准状况下,22.4LSO2气体所含的原子数为 NA | |
| D. | 常温常压下,32gO2和O3的混合气体所含原子数为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
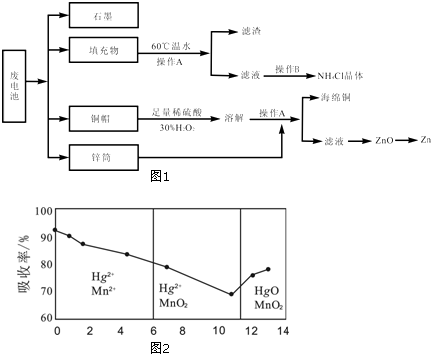
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该氢燃料充电电池是将电能转化为化学能 | |
| B. | 固态金属合金作还原剂 | |
| C. | 该电池工作过程中的总反应为H2+M═MH2 | |
| D. | 该电池反应的最终产物为H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 化学式 | 熔点(单位:℃) | 沸点(单位:℃) |
| N2 | -209.86 | -195.8 |
| O2 | -218.4 | -183 |
| CO2 | -57 | / |
| NH3 | -77.3 | -33.35 |
| Cl2 | -101 | -34.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com