
ijУ��ѧʵ����ȤС�����ʵ������ȡ����������֤������ijЩ��ѧ����ʵ�飬��ͬѧ���������ͼ��ʾ��ʵ��װ�ã�֧���õ�����̨ʡ�ԣ�����Ҫ��ش����⡣

��1�����з����У����Ƶ���������ȷ����� ��
�� MnO2��Ũ�����Ϲ��ȣ��� NaCl�����Ũ�����Ϲ��ȣ�
�� �������ƺ�ϡ�����ϣ� �� K2Cr2O7��Ũ�����ϣ�
�� KClO3��Ũ�����ϣ� �� KMnO4��Ũ�����ϡ�
A���٢ڢ� B���ڢܢ� C���٢ۢ� D���٢ܢݢ�
��2����ȡ����ʱ����ƿ�м���һ������MnO2��ͨ�� �����������ƣ�����ƿ�м���������Ũ���ᣬ�÷�Ӧ�����ӷ���ʽ�� ��ʵ��ʱΪ�˳�ȥ�����е��Ȼ������壬�����A��B֮�䰲װʢ�������������Լ��ľ���װ�á�
(3) ���ú���0.2 mol HCl��Ũ������������MnO2��Ӧ��Cl2���Ƶ�Cl2���������״���£�
����С��1.12 L��ԭ����
��4����װ��B��ʢ�� �Լ�������ţ�a.Ũ���� b.��ʯ�� c.���������� d.��ˮ�Ȼ��ơ���������
��װ��C�е������� ��D���²�Һ���������
��װ��E�з�����Ӧ�����ӷ���ʽΪ
��5����ͬѧ��Ϊ��ͬѧ��ʵ����ȱ�ݣ������ λ�ú�����ĸ������һ��װ�ã���װ����Ӧ���� �Լ�����������
��1��D (1��)��������������
�� ��2����Һ©��(1��)���� MnO2+4H++2Cl- Mn2++Cl2��+2H2O(2��) ����ʳ��ˮ(1��)
(3)Ũ�����Ũ�����ŷ�Ӧ�Ľ��б�ϡ�Ժ����ٷ�Ӧ(1��)��
����ʱŨ������ӷ�����ʧ(1��),
�� ��4��c, d (2��)��������ˮ(1��)��C�������Ա仯��������ɫ��������ɫ(1��)��
D���²����Ϻ�ɫ(1��) ,Cl2 +SO32-+H2O==2Cl- +2H++ SO42-(2��)
��5��E (1��) NaOH��Һ(1��)���� ����������ֹ��Ⱦ����(1��)��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
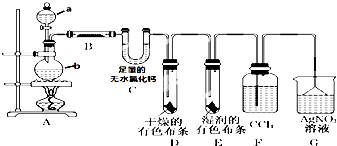 ijУ��ѧʵ����ȤС��Ϊ��̽����ʵ�����Ʊ�Cl2�Ĺ�������ˮ������HCl�ӷ�������ͬʱ֤��������ijЩ���ʣ���ͬѧ�������ͼ��ʾ��ʵ��װ�ã�֧���õ�����̨ʡ�ԣ�����Ҫ��ش����⣮��1���ٷֱ�д��a��b��ʵ����������
ijУ��ѧʵ����ȤС��Ϊ��̽����ʵ�����Ʊ�Cl2�Ĺ�������ˮ������HCl�ӷ�������ͬʱ֤��������ijЩ���ʣ���ͬѧ�������ͼ��ʾ��ʵ��װ�ã�֧���õ�����̨ʡ�ԣ�����Ҫ��ش����⣮��1���ٷֱ�д��a��b��ʵ����������
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ѡ���Լ� | ʵ������ | |
| ����1 | d d |
��Һ��ɣ�Ѫ����ɫ ��Һ��ɣ�Ѫ����ɫ |
| ����2 | b b |
�²�����Ȼ�̼��Һ��Ȼ��ɫ �²�����Ȼ�̼��Һ��Ȼ��ɫ |
| 1 |
| 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѡ���Լ�������ţ� | ʵ������ | |
| ����1 | b b |
�²㣨CCl4�㣩��ɫ �²㣨CCl4�㣩��ɫ |
| ����2 | d d |
��Һ��ΪѪ��ɫ ��Һ��ΪѪ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
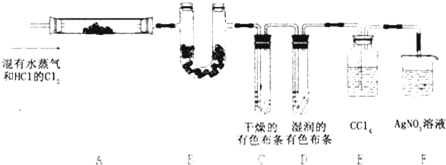
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com