
| A.0.8mol | B.l mol | C.0.2mol | D.0.4mol |
科目:高中化学 来源:不详 题型:单选题
| A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2—+4NH4++2H2O |
| B.浓烧碱溶液中加入铝片:Al+2OH-=AlO2—+H2↑ |
| C.用浓NaOH溶液溶解Al2O3:2OH-+Al2O3=2AlO2—+H2O |
| D.往碳酸镁中滴加稀盐酸:CO32—+2H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.切开的金属Na暴露在空气中,光亮表面逐渐变暗2Na+O2=Na2O2 |
| B.向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色2AgCl+S2-=Ag2S↓+2Cl- |
| C.Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物2Na2O2+2CO2=2Na2CO3+O2 |
| D.向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.能使pH试纸显蓝色的溶液中: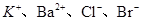 |
B.常温下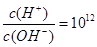 的溶液中: 的溶液中:  |
C.含有大量Al3+的溶液中: |
| D.常温下pH为7的溶液中: K+、Fe3+ 、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 >Fe3+>I2,3Br2+6FeCl2
>Fe3+>I2,3Br2+6FeCl2 2FeBr3+4FeCl3;I2+2S2
2FeBr3+4FeCl3;I2+2S2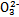
 S4
S4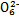 +2I-;CuI是一种白色沉淀(Ksp=1.3×1
+2I-;CuI是一种白色沉淀(Ksp=1.3×1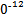 )。
)。| 实验步骤 | 实验过程和现象 | 对应结论 | |
| 步骤1 | 取一定量碘盐,用适量蒸馏水溶解,并加稀盐酸酸化,将所得试液分为3份 | _____________ | |
| 步 骤 2 | 第①份 试液 | 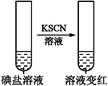 | 碘盐中肯定含 |
| 第②份 试液 | 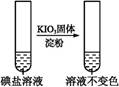 | _____________ | |
| 第③份 试液 | 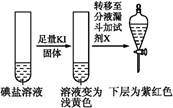 | X为 (填化学式) | |
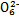 、I2、Br2的氧化性由强到弱的顺序是 。
、I2、Br2的氧化性由强到弱的顺序是 。 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.银离子 | B.亚铁离子 | C.镁离子 | D.铝离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.K+一定存在 | B.100mL溶液中含0.01mol CO32- |
| C.Cl-一定存在 | D.Ba2+一定不存在,Mg2+可能存在 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
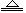 NH3↑ + H2O,NH3能使湿润的红色石蕊试纸变蓝。现某溶液中可能含有下列6种离子中的某几种:Na+、NH4+、K+、Cl-、SO42-、CO32-。为确认溶液组成进行如下实验:(1)取200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是
NH3↑ + H2O,NH3能使湿润的红色石蕊试纸变蓝。现某溶液中可能含有下列6种离子中的某几种:Na+、NH4+、K+、Cl-、SO42-、CO32-。为确认溶液组成进行如下实验:(1)取200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是| A.一定存在SO42-、CO32-、NH4+,可能存在Na+、K+、Cl- |
| B.一定存在SO42-、CO32-、NH4+、Cl-,一定不存在Na+、K+ |
| C.c(CO32-)="0.01" mol/L,c(NH4+)>c(SO42-) |
| D.如果上述6种离子都存在,则c(Cl-)>c(SO42-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
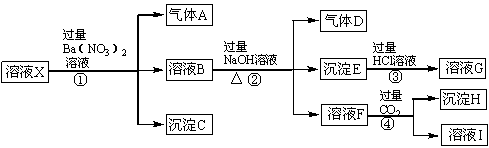
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com