
已知:还原性强弱:I->Fe2+。往100 mL碘化亚铁溶液中缓慢通入3.36 L(标准状况)氯气,反应完成后溶液中有一半的Fe2+被氧化成Fe3+。则原碘化亚铁溶液的物质的量浓度为( )

A.0.12 mol·L-1 B.0.1 mol·L-1 C.1.2 mol·L-1 D.1.0 mol·L-
科目:高中化学 来源:2016-2017学年新疆生产建设兵团二中高一上期中化学卷(解析版) 题型:填空题
相同质量的SO2和SO3的物质的量之比为___________,所含氧原子的物质的量之比为________,若欲使SO2和 SO3中氧元素的质量相等,则SO2和SO3的质量之比为___________。
SO3中氧元素的质量相等,则SO2和SO3的质量之比为___________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏林芝一中高一上期中化学试卷(解析版) 题型:选择题
约800年,波斯人炼金术士贾比尔·伊本·哈扬(Jabir ibn Hayyan)将盐酸与硝酸混合在一起发现了能够溶解金的王水。王水(aqua regia)又称“王酸”、“硝基盐酸”,是一种冒黄色雾的液体,是浓盐酸(HCl)和浓硝酸(HNO3)按体积比为3:1组成的混合物。王水一般用在蚀刻工艺和一些检测分析过程中。王水极易变质,有氯气的气味,因此必须现配现使用。请你找出适合贴在盛放有王水的药品柜上的图标( )




A B C D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上期中化学试卷(解析版) 题型:选择题
下列各组离子在溶液中能大量共存的是
A.Na+、Al3+、Cl-、SO42-
B.Cu2+、Cl-、NO3-、OH-
C.Ca2+、Na+、CO32-、NO3-
D.H+、SO42-、NO3-、OH-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高一上期中化学试卷(解析版) 题型:实验题

(1)该浓盐酸中HCl的物质的量浓度为________mol·L-1。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是________。
A.溶液中HCl的物质的量
B.溶液的浓度
C.溶液中Cl-的数目
D.溶液的密度
(3)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次 并在操作步骤空白处填上适当仪器名称)____________。
A.用30 mL水洗涤____________2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30 mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用____________加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2 cm处
(4)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”,填B表示“偏小”,填C表示“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面___________
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水___________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高一上期中化学试卷(解析版) 题型:选择题
下图是某学校实验室买回的硫酸试剂标签的部分内容。判断下列说法正确的是( )

A. 该硫酸的浓度为9.2 mol·L-1
B. 配制480 mL 4.6 mol·L-1的稀硫酸需该H2SO4125mL
C. 该硫酸与等体积水混合质量分数变为49%
D. 取该硫酸100 mL,则浓度变为原来的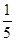
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高一上期中化学试卷(解析版) 题型:选择题
下列变化中需加入氧化剂才能实现的是( )。
A. Cl-→Cl2 B. Fe3+→Fe2+ C. CuO→Cu D. H2SO4→BaSO4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省洛阳市高一上学期期中化学试卷(解析版) 题型:选择题
300 mL A12(S04)3 溶液中,含 Al3+为 1.62 g,在该溶液中加入 0.1 mol•L-1 Ba(OH)2溶液100 mL,反应后溶液中SO42-的物质的量浓度约为
A.0.4 mol•L-1 B.0.3mol•L-1 C.0.2 mol•L-1 D.0.1 mol•L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆生产建设兵团二中高二上期中化学卷(解析版) 题型:选择题
已知某温度时CH3COOH的电离平衡常数为K。该温度下向20 mL 0.1 mol·L-1 CH3COOH溶液中逐滴加入0.1 m ol·L-1 NaOH溶液,pH变化曲线如图所示(忽略温度),以下叙述正确的是
ol·L-1 NaOH溶液,pH变化曲线如图所示(忽略温度),以下叙述正确的是
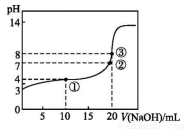
A.根据图中数据可计算出K值约为1×10-5
B.①②③点水的电离程度由大到小的顺序为:②>③>①
C.点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
D.点③时c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com