
若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是( )
|
| A. | 生成了一种强酸弱碱盐 |
|
| B. | 弱酸溶液和强碱溶液反应 |
|
| C. | 强酸溶液和弱碱溶液反应 |
|
| D. | 一元强酸溶液和一元强碱溶液反应 |
考点:
弱电解质在水溶液中的电离平衡;盐类水解的应用.
专题:
电离平衡与溶液的pH专题;盐类的水解专题.
分析:
若pH=3的酸溶液和pH=11的碱溶液中,c(H+)=c(OH﹣)=10﹣3mol/L,等体积混合后溶液呈酸性,说明应后酸过量,应为弱酸和强碱的反应,本题可讨论分析.
解答:
解:pH=3的酸溶液和pH=11的碱溶液中,c(H+)=c(OH﹣)=10﹣3mol/L,则
①若为强酸强碱,则反应后溶液呈中性,
②若为弱酸、强碱,反应后酸过量,溶液呈酸性,
③若为强酸、弱碱,则碱过量,反应后溶液呈碱性,
只有B符合,
故选:B.
点评:
本题考查弱电解质的电离和盐类的水解知识,题目难度中等,本题注意c(H+)=c(OH﹣)时,弱电解质的浓度大于强电解质溶液的浓度.


科目:高中化学 来源: 题型:
实验室用铅蓄电池作电源电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:
负极 Pb+SO42﹣═PbSO4+2e﹣
正极 PbO2+4H++SO42﹣+2e﹣═PbSO4+2H2O
今若制得Cl2 0.050摩,这时电池内消耗的H2SO4的物质的量至少是()
A. 0.025摩 B. 0.050摩 C. 0.10摩 D. 0.20摩
查看答案和解析>>
科目:高中化学 来源: 题型:
C102是一种杀菌消毒效率高、二次污染小的水处理剂.实验室中可通过以下反应制得:ClO2(其中氧元素为﹣2价)是一种消毒杀菌效率高、二次污染小的水处理剂.实验室中可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4 2ClO2↑+K2SO4+2CO2↑+2H2O下列说法不正确的是()
2ClO2↑+K2SO4+2CO2↑+2H2O下列说法不正确的是()
A. CO2是氧化产物
B. H2C2O4在反应中被氧化
C. H2C2O4的氧化性强于ClO2的氧化性
D. ClO2作水处理剂时,利用了其强氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有AgCl(s)的饱和AgCl溶液中加水,下列叙述正确的是( )
|
| A. | AgCl的溶解度增大 | B. | AgCl的溶解度、Ksp均增大 |
|
| C. | Ksp(AgCl)增大 | D. | AgCl的溶解度、Ksp均不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在pH都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH﹣离子浓度分别为Amol•L﹣1与Bmol•L﹣1,则A和B的关系为( )
|
| A. | A>B | B. | A=10﹣4B | C. | B=10﹣4A | D. | A=B |
查看答案和解析>>
科目:高中化学 来源: 题型:
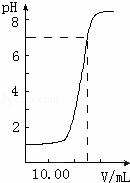
如图是向20.00mL盐酸中逐渐滴入NaOH溶液时,溶液pH值变化的图象,根据图象分析,下列结论中不正确的是( )
|
| A. | 盐酸起始浓度为0.1mol•L﹣1 |
|
| B. | NaOH溶液浓度为0.08mol•L﹣1 |
|
| C. | 滴入碱量为20mL时,向混合溶液中滴入2滴甲基橙试液,溶液显橙色 |
|
| D. | 滴到中和点时,耗NaOH物质的量为0.002mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
在理论上不能用于设计原电池的化学反应是( )
|
| A. | 2FeCl3(aq)+2KI(aq)═2FeCl2(aq)+2KCl(aq)+I2(aq)△H<0 |
|
| B. | Ba(OH)2•8H2O(s)+2NH4Cl(s)═BaCl2(aq)+2NH3•H2O(aq)+8H2O(l)△H>0 |
|
| C. | 4Al(s)+6H2O(l)+3O2(g)═4Al(OH)3(s)△H<0 |
|
| D. | Zn(s)+2MnO2(s)+2H2O(l)═2MnOOH(s)+Zn(OH)2(s)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
等质量的两份锌粉a、b分别加入到两份质量相同的过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,下列各图为产生H2的体积V(L)与时间t(min)的关系,其中正确的是( )
|
| A. |
| B. |
| C. |
| D. |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
安全是顺利进行实验及避免伤害的保障.下列实验操作正确且不是从实验安全角度考虑的是()
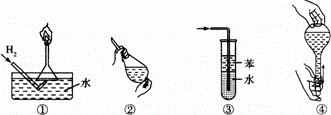
A. 操作①:使用稍浸入液面下的倒扣漏斗检验氢气的纯度
B. 操作②:使用CCl4萃取溴水中的溴时,振荡后需打开活塞使漏斗内气体放出
C. 操作③:吸收氨气或氯化氢气体并防止倒吸
D. 操作④:用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立,检查容量瓶是否漏水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com