
��50 mL 0.50 mol/L��������50 mL 0.55 mol/L������������Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺

��1���ձ�����������ĭ���ϵ�������___________________________
��2�����β���������ܷ��û������ʽ�������棿_____(��ܡ����ܡ�)��
��ԭ����_______________________________________________________��
��3��ʵ��ʱ����������Һ��Ũ��Ҫ��0.55 mol/L��ԭ����______________________��
ʵ����������60 mL 0.50 mol/L��������50 mL 0.55 mol/L������������Һ���з�Ӧ�� ������ʵ����ȣ����ų�������_______ _____(���ȡ�������ȡ�)����ʵ���������ȷ���������к���________________(���ȡ�������ȡ�)��
��4����֪��ϡ��Һ�У�ǿ���ǿ����кͷ�Ӧ����1 mol H2Oʱ���ų�57.3 kJ����������������Ӧ���Ȼ�ѧ����ʽΪ��__________________________________��
 ����ͼ���������������ϵ�д�
����ͼ���������������ϵ�д� ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��������ͼװ�ý���ʵ�飬��ʼʱ��a��b����Һ����ƽ���ܷ�ã�����һ��ʱ�䡣����˵������ȷ����
��������ͼװ�ý���ʵ�飬��ʼʱ��a��b����Һ����ƽ���ܷ�ã�����һ��ʱ�䡣����˵������ȷ����
A��a�ܷ���������ʴ��b�ܷ������ⸯʴ
B��һ��ʱ���a��Һ�����b��Һ��
C��a����Һ��pH����b����Һ��pH��С
D��a��b����������ͬ�ĵ缫��Ӧʽ��Fe��2e��===Fe2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ᱽ�����м�ǿ�Ŀ��Ϳ��������Զ������������á�����Ƴ�����·�ߺϳɻ���ҩ��ۿ����ᱽ������

��֪��B�ĺ˴Ź����������������壻���������ʾ����������д���̼̼˫�����ң�


�ش����и��⣺
(1)����B�����ƣ�________(ϵͳ������)��
(2)���������C��H��O����Ԫ�أ������ܶ�����ͬ������H2��90����������������Ϊ35.6%������ķ���ʽΪ________�����������NaHCO3��Һ��Ӧ�������壬1 mol�������������Ʒ�Ӧ����1.5 mol H2�������������к��������ŵ����ƣ�________��
(3)д�����з�Ӧ�����ͣ���__________����___________________________��
(4)д����Ӧ�۵Ļ�ѧ����ʽ��_______________________________________��
(5)�������������Ŀ������ͬ���칹����________�֡�
�ٺ��������Ȼ����ڱ�����������ȡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ͭпԭ���(��ͼ)����ʱ������������ȷ���� (����)
A��������ӦΪ��Zn��2e��===Zn2��
B����ط�ӦΪ��Zn��Cu2��===Zn2����Cu
C�������·�У����Ӵ���������
D�������е�K������ZnSO4��Һ

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ͬ��ͬѹ�£���֪���и���Ӧ��Ϊ���ȷ�Ӧ�����з������ٵ��ǣ� ��
A��2A ( l ) + B ( l ) = 2C ( g ) ��H1 B��2A ( g ) + B ( g ) = 2C ( g ) ��H2
C��2A ( g ) + B ( g ) = 2C ( l ) ��H3 D��2A ( l ) + B ( l ) = 2C ( l ) ��H4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ij�ܱ������м���0.6 mol A�� 0.2 mol C��һ������B�������塣һ�������·�����Ӧ��������Ũ����ʱ��仯���ͼ��ʾ[����t0��t1��c(B)δ����]��t2ʱ�̺�ı�������Ӧ��ϵ�з�Ӧ������ʱ��仯���������ͼ��ʾ�����ĸ��ζ����ı�һ���������Ҹı������������ͬ������˵����ȷ����
0.2 mol C��һ������B�������塣һ�������·�����Ӧ��������Ũ����ʱ��仯���ͼ��ʾ[����t0��t1��c(B)δ����]��t2ʱ�̺�ı�������Ӧ��ϵ�з�Ӧ������ʱ��仯���������ͼ��ʾ�����ĸ��ζ����ı�һ���������Ҹı������������ͬ������˵����ȷ����

A����Ӧ�ķ���ʽΪ3A(g)��B(g)  2C(g)
2C(g)
B��t3��t4��t4��t5��t5��t6���ο��ܸı����������Ϊ���Ӵ��������ͷ�Ӧ�¶ȣ�����ѹǿ
C��B����ʼ���ʵ���Ϊ0.08 mol
D����t1��10 s��A��t0��t1ʱ��εķ�Ӧ����Ϊ0.002 25 mol��L��1��s��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ϳɰ���Ӧ��N2(g)��3H2(g)  2NH3(g)����H����92.4 kJ�� mol��1���ڷ�Ӧ�����У�����Ӧ���ʵı仯��ͼ��
2NH3(g)����H����92.4 kJ�� mol��1���ڷ�Ӧ�����У�����Ӧ���ʵı仯��ͼ��

����˵����ȷ����
A��t1ʱ�������¶ȡ������� B��t2ʱʹ���˴���
C��t3ʱ������ѹǿ D��t4ʱ�������¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���½�����ұ�������ڹ�ҵ�ϲ����õ���(����)
A��Fe2O3��3CO 2Fe��3CO2
2Fe��3CO2
B��Al2O3��3CO 2Al��3CO2
2Al��3CO2
C��MgCl2(����) Mg��Cl2��
Mg��Cl2��
D��2HgO 2Hg��O2��
2Hg��O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����л����У���ͭ�������´�����,���ܷ�����ȥ��Ӧ������ȥ�������д���ͬ���칹�����:
A.CH3 CH2C(OH)(CH3��2 B.��CH3��2CHOH
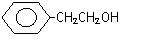 C . CH3CH��OH��CH2 CH3 D.
C . CH3CH��OH��CH2 CH3 D.
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com