
(11分)在实验室里用乙醇跟浓H2SO4反应制取乙烯时,常因温度过高而发生副反应,部分乙醇跟浓H2SO4反应生成SO2,CO2,水蒸气和炭黑。
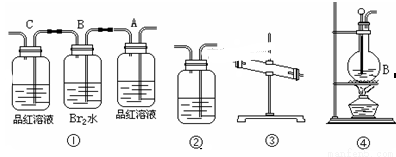
(1)用编号为①→④ 的实验装置设计一个实验,以验证上述反应混合气体中含CO2,SO2和水蒸气。用装置的连接顺序(按产物气流从左到右的流向):
→ → → →。
(2)实验的装置①中A瓶的现象是________;结论为______________。
B瓶中的现象是________;B瓶溶液作用为________;
是否能将B瓶溶液换成酸性高锰酸钾______ (答是,否)。
(3)装置③中加的固体药品是________装置②中盛的溶液是________。
(4)装置④生成乙烯的反应类型是______ ;若要验证混合气体中有乙烯,应将混合气体先通过盛____________的洗气瓶,再通过盛______ 的试管中。
(1)4→ 3 → 1 → 2 →;
(2)A瓶退色;含SO2;颜色变浅;吸收SO2(乙烯可答可不答);否;
(3)无水CuSO4,澄清石灰水;
(4)消去反应;NaOH溶液;溴水或酸性高锰酸钾溶液;
【解析】
试题分析:(1)检验二氧化硫用品红溶液,检验二氧化碳用澄清的石灰水,检验水蒸气用无水硫酸铜,因溶液中有水,所以首先检验水蒸气;因为CO2是用澄清石灰水来检验的,而SO2也可以使澄清石灰水变浑,二氧化硫能使品红褪色,二氧化碳不能,所以,检验二氧化硫在检验二氧化碳之前,再通过澄清石灰水确认CO2存在;(2)实验时装置①的作用是检验二氧化硫的存在并除去二氧化硫,A瓶中装有品红溶液,二氧化硫能使品红褪色,所以现象是品红褪色,说明混合气中有SO2;B装置吸收SO2,SO2+Br2+2H2O=2H2SO4+2HBr,现象是橙色褪去;C装置品红不褪色,说明SO2吸收完全。(3)装置③的作用是检验水蒸气,用白色的无水硫酸铜粉末,CuSO4+5H2O═CuSO4?5H2O变蓝说明混合气体中有水蒸气;装置②的作用是检验二氧化碳,用澄清石灰水,Ca(OH)2+CO2=CaCO3↓+H2O,澄清石灰水变浑浊,确认CO2存在。(4)装置④生成乙烯的反应类型是消去反应;若要验证混合气体中有乙烯,应将混合气体先通过盛NaOH溶液的洗气瓶,再通过盛溴水或酸性高锰酸钾溶液的试管中。
考点:考查乙醇跟浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和炭黑产物的检验,注意当有多种产物需检验时,应考虑先后顺序。


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源:2013-2014广东省惠州市高一下学期期末考试化学(理)试卷(解析版) 题型:选择题
下列化合物中,不属于有机物的是
A.甲烷 B.淀粉 C.二氧化碳 D.蔗糖
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省高三5月第三次模拟理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.糖类化合物都具有相同的官能团 B.酯类物质是形成水果香味的主要成分
C.油脂的皂化反应生成脂肪酸和丙醇 D.蛋白质的水解产物都含有羧基和羟基
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省佛山市高三教学质量检测二理综化学试卷(解析版) 题型:选择题
已知醋酸、醋酸根离子在溶液中存在下列平衡及其对应的平衡常数
CH3COOH CH3COO— + H+ K1=1.75×10-5 △H1>0
CH3COO— + H+ K1=1.75×10-5 △H1>0
CH3COO— + H2O CH3COOH + OH— K2=5.71×10-10 △H2>0
CH3COOH + OH— K2=5.71×10-10 △H2>0
常温下,将等体积、等物质的量浓度的醋酸和醋酸钠溶液混合,下列叙述正确的是
A.对混合溶液进行微热,K1增大、K2减小
B.混合溶液的pH<7
C.混合溶液中c(CH3COO—)>c(Na+)
D.温度不变,若在混合溶液中加入少量NaOH固体,c(CH3COO—)减小
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省佛山市高三教学质量检测二理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.淀粉、油脂、氨基酸都能水解,但水解产物不同
B.甲醛可用作食品防腐剂
C.植物油和裂化汽油都能使溴水褪色
D.对“地沟油”进行分馏可以制得汽油、煤油,达到变废为宝的目的
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省高二下学期期中化学试卷(解析版) 题型:选择题
下列有机物中含有的杂质(括号内为杂质),可用稀NaOH溶液作试剂并采用分液的方法除去的是
A.苯(溴) B.淀粉(葡萄糖)
C.甲苯(苯酚) D.苯甲酸(苯酚)
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省高二下学期期中化学试卷(解析版) 题型:选择题
在下列有关说法中正确的是
①相同质量的CH4、C2H4、C2H2完全燃烧时耗O2量的关系为CH4 > C2H4 >C2H2
②对于任意比混合的乙烯、丙烯和环丁烷混合气体在足量氧气中燃烧,只要混合气体的质量不变,完全燃烧后产生的CO2和H2O的量也不改变
③对于任意比混合的C2H4、C2H6、C2H2混合气体,只要混合气体物质的量不变,完全燃烧后产生的CO2物质的量也不改变
④某有机物在足量氧气中燃烧后产生CO2与H2O的物质的量之比为2:3,则该有机物的类型肯定为烷烃
A.①②③B.①②③④C. ②③D.以上组合均不正确
查看答案和解析>>
科目:高中化学 来源:2013-2014广东清远市市高二下学期期末考试化学试卷(解析版) 题型:选择题
有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列各项事实不能说明上述观点的是
A.甲苯能使酸性高锰酸钾溶液褪色,而甲烷不能使高锰酸钾酸性溶液褪色
B.乙烯能发生加成反应,而乙烷不能发生加成反应
C.苯酚能和氢氧化钠溶液反应,而乙醛不能和氢氧化钠溶液反应
D.苯酚苯环上的氢比苯分子中的氢更容易被卤原子取代
查看答案和解析>>
科目:高中化学 来源:2013-2014广东佛山市顺德区高三5月教学质量检测理综化学试卷(解析版) 题型:填空题
(16分)卤块的主要成分是MgCl2,此外还含Fe2+、Fe3+和Mn2+等杂质离子。以卤块为原料按下图所示流程进行生产,可制得轻质氧化镁。

查阅资料得下表相关数据:
表1: 生成氢氧化物沉淀的pH | 表2: 原料价格表 | |||
物质 | 开始沉淀 | 沉淀完全 | 物质 | 价格(元/吨) |
Fe(OH)3 | 2.7 | 3.7 | a.漂液(含25.2%NaClO) | 450 |
Fe(OH)2 | 7.6 | 9.6﹡ | b.双氧水(含30%H2O2) | 2400 |
Mn(OH)2 | 8.3 | 9.8 | c.烧碱(含98%NaOH) | 2100 |
Mg(OH)2 | 9.6 | 11.1 | d.纯碱(含99.5%Na2CO3) | 600 |
﹡Fe2+氢氧化物呈絮状,不易从溶液中除去,必须将它氧化后以Fe(OH)3沉淀形式才能除尽。
若要求产品尽量不含杂质且生产成本较低,请根据上表提供的资料回答:
(1)流程中加入的试剂X、Y、Z最佳选择依次是表2中的 (选填试剂编号)。
(2)步骤②发生反应的离子方程式为 ;步骤⑤中发生反应的化学方程为 。
(3)步骤③控制pH=9.8的目的是 。
(4) 若在实验室进行步骤⑥的灼烧实验,必须用到的仪器是铁三脚、酒精喷灯、 和
泥三角。
(5)在探究Mg(OH)2溶解性的实验中,发现向装有少量Mg(OH)2浊液的试管中加入适量
NH4Cl晶体,充分振荡后溶液会变澄清,请用化学平衡的原理解释浊液变澄清的原
因 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com