
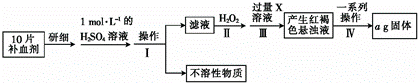
分析 (1)Fe3+遇KSCN溶液显红色,该现象用于检验Fe3+存在,证明操作Ⅰ滤液中含有Fe2+的方法之一是向滤液中加入NaOH溶液反应生成白色沉淀迅速变化为灰绿色,最后变化为红褐色;过氧化氢氧化亚铁离子;
(2)步骤④中一系列处理是由氢氧化铁悬浊液最终转化为氧化铁,需要过滤、洗涤的氢氧化铁,然后灼烧生成氧化铁,冷却后称量氧化铁的质量;
(3)根据氧化铁的质量计算铁元素的质量.注意ag氧化铁含有的铁元素质量为10片含有的铁元素质量;
(4)①用酸性KMnO4溶液滴定也能进行铁元素含量的测定,是利用高锰酸钾溶液氧化亚铁离子定量关系测定;
②精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻棒、烧杯、胶头滴管,250mL容量瓶;
③KMnO4溶液需要酸化,用于酸化的酸不能具有强氧化性氧化Fe2+,不能具有强还原性被高锰酸钾氧化,否则会影响高锰酸钾溶液的体积;
④高锰酸钾为紫色,当滴定到终点时,Fe2+被完全氧化,加入的最后一滴高锰酸钾不反应,依据离子方程式定量关系计算亚铁离子物质的量,得到铁元素质量分数;
解答 解:(1)Fe3+遇KSCN溶液显红色,该现象用于检验Fe3+存在,证明操作Ⅰ滤液中含有Fe2+的方法之一是向滤液中加入NaOH溶液,生成白色沉淀,白色沉淀迅速变为灰绿色,最终变为红褐色,步骤Ⅱ中发生反应是亚铁离子被过氧化氢氧化生成铁离子,反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O;
故答案为:生成白色沉淀,白色沉淀迅速变为灰绿色,最终变为红褐色,2Fe2++H2O2+2H+=2Fe3++2H2O;
(2)步骤④中一系列处理是由氢氧化铁悬浊液最终转化为氧化铁,需要过滤、洗涤的氢氧化铁,然后灼烧生成氧化铁,冷却后称量氧化铁的质量,
故答案为:洗涤;冷却;
(3)最后氧化铁为ag,氧化铁含有铁元素的质量为$\frac{112}{160}$×ag=0.7ag,故每片补血剂含铁元素的质量为$\frac{0.7a}{10}$=0.07ag,
故答案为:0.07a;
(4)①用酸性KMnO4溶液滴定也能进行铁元素含量的测定,是利用高锰酸钾溶液氧化亚铁离子定量关系测定,反应的离子方程式为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
故答案为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
②精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻棒、烧杯、胶头滴管,250mL容量瓶,
故答案为:250mL容量瓶;
③稀硝酸、浓硝酸具有强氧化性,含有氧化Fe2+,高锰酸钾可以氧化HCl为氯气,故选硫酸酸化,故选:b;
④高锰酸钾为紫色,当滴定到终点时,Fe2+被完全氧化,加入的最后一滴高锰酸钾不反应,依据离子方程式定量关系计算亚铁离子物质的量,得到铁元素质量分数;
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
5 1
n 0.1mol•L-1 ×0.1L
n=0.05mol
该补血剂中铁元素的质量分数=$\frac{0.05mol×56g/mol}{mg}$×100%=$\frac{2.8}{m}$×100%;
故答案为:$\frac{2.8}{m}$×100%.
点评 本题考查学生对实验原理与实验操作的理解、物质分离提纯、元素化合物性质、化学计算等、氧化还原滴定应用,难度中等,清楚实验原理是解题的关键,需要学生具备扎实的基础知识与综合运用知识分析问题、解决问题的能力.


科目:高中化学 来源: 题型:解答题
| 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| 步骤I: ① . 步骤II:配制与0.1 mol/L Fe(NO3)3 溶液所含c (H+)、 c (NO3-) 相同的溶液,取适量此溶液放入到新制备的银镜中. | ② ,乙同学的推测 成立;反之,则不成立. |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.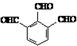 .
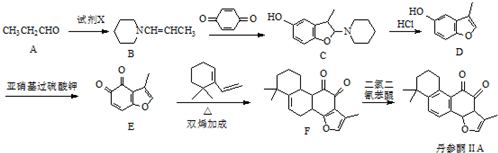
.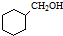 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌粒与稀盐酸反应:Zn+2H+═Zn2++H2↑ | |
| B. | 碳酸钙与盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| C. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 稀醋酸与氢氧化钠溶液的反应:H++OH-═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将作物秸秆通过化学反应转化为乙醇用作汽车燃料 | |
| B. | 使用资源节约型、环境友好型的生物降解塑料包装袋 | |
| C. | 大力研发新型有机溶剂替代水作为萃取剂 | |
| D. | 利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
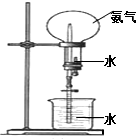 如图所示,在干燥的圆底烧瓶里充满氨气,用带有玻璃管和滴管(滴管里预先吸入水)的塞子塞紧瓶口.立即倒置烧瓶,使玻璃管插入盛有水的烧杯里(预先在水里滴入少量酚酞溶液).打开橡皮管上的夹子,轻轻挤压滴管,使少量水进入烧瓶,可观察到的现象为:烧杯里的水由玻璃管进入烧瓶,形成喷泉,烧瓶内液体呈红色.
如图所示,在干燥的圆底烧瓶里充满氨气,用带有玻璃管和滴管(滴管里预先吸入水)的塞子塞紧瓶口.立即倒置烧瓶,使玻璃管插入盛有水的烧杯里(预先在水里滴入少量酚酞溶液).打开橡皮管上的夹子,轻轻挤压滴管,使少量水进入烧瓶,可观察到的现象为:烧杯里的水由玻璃管进入烧瓶,形成喷泉,烧瓶内液体呈红色.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═[Al(OH)4]-+4NH4+ | |
| B. | MgSO4溶液中加入Ba(OH)2溶液:SO42-+Ba2+=BaSO4↓ | |
| C. | 硫化钠溶液显碱性:S2-+2H2O═H2S+2OH- | |
| D. | NaHCO3溶液加入少量Ca(OH)2溶液:2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO3-、SO42-、NH4+、Mg2+ | B. | Cu2+、Mg2+、Cl-、SO42- | ||
| C. | H+、K+、OH-、NO3- | D. | Ag+、Na+、NO3-、CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com