
| A. | 使用前要先检查容量瓶是否漏液 | |
| B. | 用蒸馏水洗涤后必须要将容量瓶烘干 | |
| C. | 为了方便快捷,可以直接在容量瓶内进行固体溶解 | |
| D. | 定容结束后,为了使溶液均匀,手握瓶颈,左右振荡 |
分析 A.容量瓶使用前需要检查是否漏液;
B.容量瓶中有少量水对实验无影响;
C.不能在容量瓶中溶解固体;
D.摇匀时上下颠倒.
解答 解:A.容量瓶使用前需要检查是否漏液,若漏液不能使用,则使用前要先检查容量瓶是否漏液,故A正确;
B.容量瓶中有少量水对实验无影响,则用蒸馏水洗涤后,容量瓶不需要烘干,故B错误;
C.不能在容量瓶中溶解固体,应在烧杯中溶解、冷却后转移到容量瓶中,故C错误;
D.定容结束后,为了使溶液均匀,手握瓶颈,上下颠倒来振荡,不能左右振荡,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握常见仪器的使用、溶液配制、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中加入CCl4,CCl4层显紫色,说明原溶液中存在I- | |
| B. | 某溶液中滴加NaOH生成白色沉淀,迅速变成灰绿色,最终变成红褐色,则原溶液有Fe2+,无Fe3+ | |
| C. | 将CO2通入某溶液中,不能产生白色沉淀,说明原溶液中不含Ba2+或Ca2+ | |
| D. | 用干净的铂丝蘸取某溶液在酒精灯外焰上灼烧,火焰呈黄色,说明该溶液中有Na+无K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
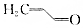 .则与键线式为
.则与键线式为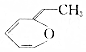 的物质互为同分异构体的是( )
的物质互为同分异构体的是( )| A. |  | B. |  | C. | 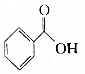 | D. | 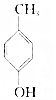 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分别配成溶液,再加入澄清石灰水 | |
| B. | 分别取固体样品,滴加同浓度盐酸,观察产生气泡的快慢 | |
| C. | 分别加热,再检验是否有使澄清石灰水变浑浊的气体产生 | |
| D. | 在两只试管中分别加入各约1 g的两种固体和10 mL水,振荡后分别滴入2滴酚酞 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | a | b | c | 试管②中现象 | 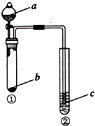 |
| A | NaOH溶液 | Al | 肥皂水 | 肥皂泡可点燃 | |
| B | 稀盐酸 | 碳酸钙 | NaAlO2溶液 | 生成白色絮状沉淀生成 | |
| C | 稀硫酸 | NaHCO3 | BaCl2溶液 | 溶液变浑浊 | |
| D | 水 | Na2O2 | 酸化的FeSO4溶液 | 溶液变黄 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | D溶液的pH=7 | |
| B. | 四种溶液相比,C溶液中水的电离程度最大 | |
| C. | A与C等体积混合后,溶液中有c(Cl-)>c(H+)>c(NH4+)>c(OH-) | |
| D. | B与D等体积混合后,溶液中有c(OH-)=c(CH3COOH)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知CH3OH(l)的燃烧热为238.6 kJ•mol-1,则CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(g)△H=-238.6 kJ•mol-1 | |
| B. | 钢铁水闸可用牺牲阳极或外加电流的阴极保护法防止其腐蚀 | |
| C. | 反应H2+Cl2═2HCl(△H<0)的机理包含①Cl2-→2Cl(慢),②H2+Cl-→HCl+H(快),③Cl2+H-→HCl+Cl(快),则反应①的活化能小于反应②的活化能 | |
| D. | 一定条件下反应N2+3H2?2NH3达到平衡时,3v正(H2)=2v逆(NH3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
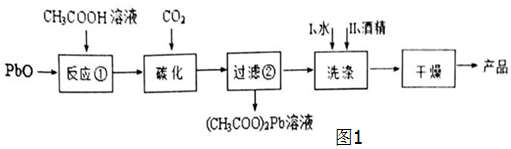
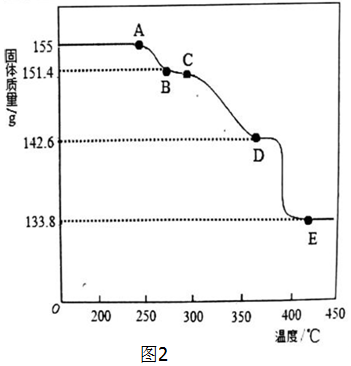
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com