
��-���Ȼ�ѧѭ������ʾ��ͼ���£�
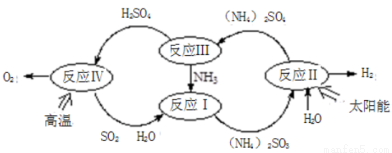
��1����Ӧ���ǽ�̫����ת��Ϊ���ܣ���ת��Ϊ��ѧ�ܣ����������ĵ缫��Ӧʽ _______________;
��2����Ӧ���п��Ʒ�Ӧ��������Ҫ����ͬ����������立ֽ���ﲻͬ������װ��A-B-C����������ԣ���ͼʾ���¼����Լ���ͨ��N2�ž���������400�����װ��A ��(NH4)2SO4��ȫ�ֽ������ֹͣ���ȣ���ȴ��ֹͣͨ��N2���۲쵽װ��A��B֮��ĵ���������������ɫ���塣�����飬�ð�ɫ�����װ��B����Һ����SO32-����SO42-����һ���о����֣�����������������
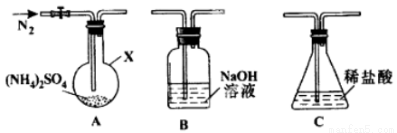
(NH4)2 SO4��400��ֽ�Ļ�ѧ����ʽ��:________________________________________;
��3����Ӧ����2H2SO4(l)=2SO2(g)+O2(g)+2H2O (l) ��H=+462kJ/mol
����������Ӧ��ɣ�i��H2SO4(l)=SO3(g)+H2O(g) ��H=+177kJ/mol
ii��SO3(g)�ֽ⡣
iii.H2O(l)=H2O(g) ��H=+44kJ/mol
��L(L1��L2)��X�ɷֱ����ѹǿ���¶ȡ���ͼ��ʾ Lһ��ʱ��ii��SO3(g)��ƽ��ת������X�ı仯��ϵ��
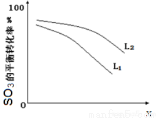
i��X�������������ǣ�________________,
ii���ж�L1��L2�Ĵ�С��ϵ�����������ɣ�________________________________________;
�ڷ�SO3�ֽ���Ȼ�ѧ����ʽΪ��__________________________________________________;
��4�������ܱ������У����Ʋ�ͬ�¶Ƚ���SO3�ֽ�ʵ�顣SO3��ʼŨ�Ⱦ�Ϊ cmol��L��1���ⶨSO3��ת���ʣ������ͼ��ͼ�Т�����ΪSO3��ƽ��ת�������¶ȵĹ�ϵ�������߱�ʾ��ͬ�¶��·�Ӧ������ͬ��Ӧʱ����δ�ﵽ��ѧƽ��ʱSO3��ת���ʡ�
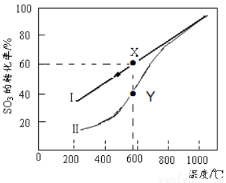
��ͼ�е�X��ƽ�ⳣ����K=_____ ��
��Y���Ӧ�¶��µķ�Ӧ���ʣ�v(��)______v(��)(ѡ�����������)�����¶ȵ����ߣ������߱ƽ������ߵ�ԭ���ǣ�_____________________________________��
 ѧ���쳵�����ּ��������ҵ�½����������ϵ�д�
ѧ���쳵�����ּ��������ҵ�½����������ϵ�д� �����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д� Сѧ�����ҵ���ϴ�ѧ������ϵ�д�
Сѧ�����ҵ���ϴ�ѧ������ϵ�д� ���Ž�����ٰθ��νӹ㶫���������ϵ�д�
���Ž�����ٰθ��νӹ㶫���������ϵ�д� �����������ҵ�������������ϵ�д�
�����������ҵ�������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�����и�һ����ĩ���ƻ�ѧA���������棩 ���ͣ�ѡ����
��ͼ�Dz��ֶ�����Ԫ��ԭ�ӣ�����ĸ��ʾ��������������ԭ�������Ĺ�ϵͼ������˵����ȷ���ǣ� ��

A. X��R��ͬһ����
B. ԭ�Ӱ뾶��W��R��X
C. ��̬�⻯����ȶ��ԣ�Y��X
D. X��Z�γɵĻ�������ֻ�����Ӽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶��µڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���и���ʵ��������������ó��Ľ�����ȷ����
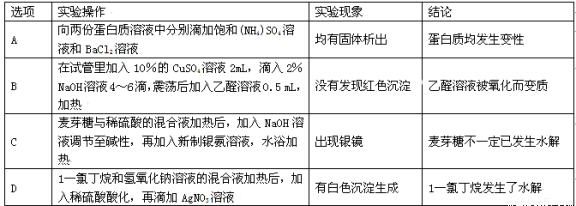
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�켪��ʡ����ʮһ�����¿�ǰ������ۻ�ѧ�Ծ����������棩 ���ͣ������
������(H3PO2)��һ�־�ϸ������Ʒ�����н�ǿ��ԭ�ԣ��ش��������⣺
��1��H3PO2��һԪ��ǿ�ᣬд������뷽��ʽ��___________��
��2��H3PO2��NaH2PO2���ɽ���Һ�е������ӻ�ԭΪ�����ʣ��Ӷ������ڻ�ѧ������
��(H3PO2)�У���Ԫ�صĻ��ϼ�Ϊ___________��
������(H3PO2)���л�ѧ������Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ4:1������������Ϊ��___________(�ѧʽ)��
��NaH2PO2�� ���λ�����ʽ�Σ�___________������Һ��___________��(������ԡ��������ԡ������ߡ������ԡ�)��
��3��H3PO2�Ĺ�ҵ�Ʒ��ǣ�������(P4)������������Һ��Ӧ����PH3�����Ba(H2PO2)2�������������ᷴӦ��д������������������Һ��Ӧ�Ļ�ѧ����ʽ___________��
��4��(H3PO2)Ҳ����ͨ�����ķ����Ʊ�������ԭ����ͼ��ʾ(��Ĥ����Ĥ�ֱ�ֻ���������ӡ�������ͨ��):
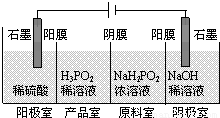
��д�������ĵ缫��Ӧʽ___________��
�ڷ�����Ʒ�ҿɵõ�H3PO2��ԭ��___________��
�����ڲ��á����ҵ����������Ʊ�H3PO2���������ҵ����������������ҵ�ϡ������H3PO2ϡ��Һ���棬����ȥ���������Ʒ��֮�����Ĥ���Ӷ��ϲ������������Ʒ�ң���ȱ����___________���ʡ������ʲ�����ԭ����___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�켪��ʡ����ʮһ�����¿�ǰ������ۻ�ѧ�Ծ����������棩 ���ͣ�ѡ����
Wolff-Kishner-��������Ӧ��ȩ���ͪ���ڼ����������������ã�ʹ��>C=Oת��Ϊ-CH2-���磺
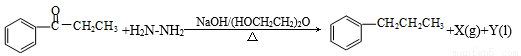
���У�X��Y����Ⱦ����������˵���в���ȷ����( )
A��������ԭ��
B��X��N2
C��Y��H2O
D��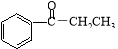 ������������ˮ��Ϊ��������Ҵ�
������������ˮ��Ϊ��������Ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʡ������ҵ�����һ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����Ʒӵ�һ�ֺϳ�·����ͼ��������������ȷ����( )
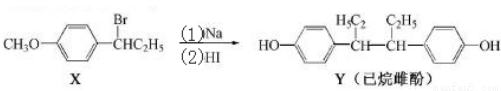
A��������X �ķ���ʽΪC9H13BrO B��������X�����ϵ�һ�����������
C����FeCl3��Һ�ɼ�����X��Y D����Ӧ��2������ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�߶�5���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
������ͭ�Ǻϳ��������������в��ϡ�����������ͭ����Ҫǰ��֮һ������������һ��ʵ���Һϳ�·�ߣ�
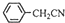 +H2O+H2SO4
+H2O+H2SO4
 +NH4HSO4
+NH4HSO4
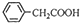 +Cu(OH)2��(
+Cu(OH)2��(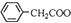 )2Cu+H2O
)2Cu+H2O
��֪����������۵�Ϊ-23�棬������ˮ��
��������۵�Ϊ76.5�棬������ˮ�������Ҵ���
�ش��������⣺
��1���Ʊ��������װ��ʾ��ͼ��ͼ(���Ⱥͼг�װ�õ���)����250mL����ƿa�м���70mL 70%���ᣮ���ƴ�����ʱ����������ˮ��Ũ������Ⱥ�˳����__________��
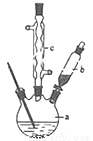
��2����a�е���Һ������100�棬����b�����μ�40g�����浽������Һ�У�Ȼ��������130�������Ӧ����װ���У�����c��������__________����������__________��
��3����Ӧ�������������ˮ���ٷ�����������Ʒ��������ˮ��Ŀ����__________�����������п����ڷ��뱽�����Ʒ����__________��
A����Һ©�� |
B��©�� |
C���ձ� |
D��ֱ�������� |
E��������
��4���ᴿ������ķ�����__________�����յõ�44g��Ʒ��������IJ�����__________��
��5������������뵽�Ҵ���ˮ�Ļ���ܼ��У�����ܽ����Cu(OH)2����30min�����ˣ���Һ����һ��ʱ�䣬����������ͭ���壬����ܼ����Ҵ���������__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�߶�5���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA��ʾ������������ֵ������˵����ȷ����
A�������£�1L0.1mol•L-1CuSO4��Һ�к��е�Cu2+��ĿΪ0.1NA
B����1molCl-��NH4Cl��Һ�м���������ˮʹ��Һ�����ԣ���ʱ��ҺNH4+ΪNA
C��2mol SO2�������������ʵ��������·�Ӧ����SO3��ת�Ƶĵ�����Ϊ4NA
D��25��Cʱ��1L pH=1��������Һ�У�����H+����ĿΪ0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣��ʡ��һ�µڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪H+(aq)+OH��(aq)=H2O(l)�ų���57.3KJ,���з�Ӧ�зų�57.3KJ�������� ( )
��KHSO4(aq)+KOH(aq)= K2SO4(aq)+ H2O(l) ��H2SO4(aq)+Ba(OH)2=BaSO4��+2 H2O(l)
��HCl(aq)+ NaOH(aq)=NaCl (aq)+ H2O(l) ��HCl(aq)+NH3��H2O(aq)=NH4Cl(aq)+ H2O(l)
��H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2 H2O(l) ��CH3COOH(aq)+NaOH(aq)= CH3COONa(aq)+ H2O(l)
A�٢� B���ۢ� C���ܢ� D���ڢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com