
| A£® | ČÜŅŗµÄÅØ¶Č±äĪŖ0.08mol/L | B£® | Ńō¼«ÉĻ²śÉś112ml O2 £Ø±ź×¼×“æö£© | ||
| C£® | ×ŖŅʵĵē×ÓŹżŹĒ1.204”Į1022 øö | D£® | ·“Ó¦ÖŠÓŠ0.01mol Ag ±»Ńõ»Æ |
·ÖĪö 1L 0.1mol/LµÄAgNO3ČÜŅŗŌŚŅŌAg×÷Ńō¼«£¬Fe×÷Ņõ¼«µÄµē½ā²ŪÖŠµē½ā£¬Ńō¼«·“Ó¦Ź½ĪŖAg-e-=Ag+”¢Ņõ¼«·“Ó¦Ź½ĪŖ Ag++e-=Ag£¬ĖłŅŌøĆ×°ÖĆŹĒµē¶Ę³Ų£¬µē¶ĘŹ±µē½āÖŹČÜŅŗÅØ¶Č²»±ä£¬½įŗĻAgŗĶ×ŖŅʵē×ÓÖ®¼ä¹ŲĻµŹ½·ÖĪö½ā“š£®
½ā“š ½ā£ŗ1L 0.1mol/LµÄAgNO3ČÜŅŗŌŚŅŌAg×÷Ńō¼«£¬Fe×÷Ņõ¼«µÄµē½ā²ŪÖŠµē½ā£¬Ńō¼«·“Ó¦Ź½ĪŖAg-e-=Ag+”¢Ņõ¼«·“Ó¦Ź½ĪŖ Ag++e-=Ag£¬ĖłŅŌøĆ×°ÖĆŹĒµē¶Ę³Ų£¬
A£®ŅņĪŖČܽāµÄAgŗĶĪö³öµÄAgÖŹĮæĻąµČ£¬ĖłŅŌµē½āÖŹČÜŅŗÅØ¶Č²»±ä£¬ČŌČ»ĪŖ1mol/L£¬¹ŹA“ķĪó£»
B£®½Ļ»īĘĆ½šŹō×÷Ńō¼«£¬Ńō¼«ÉĻ½šŹōŹ§µē×Ó£¬ĖłŅŌŃō¼«·“Ó¦Ź½ĪŖAg-e-=Ag+£¬¹ŹB“ķĪó£»
C£®øł¾ŻAg-e-=Ag+ÖŖ£¬Īö³ö2.16gAgŹ±×ŖŅʵē×ÓŹż½ā£ŗ1L 0.1mol/LµÄAgNO3ČÜŅŗŌŚŅŌAg×÷Ńō¼«£¬Fe×÷Ņõ¼«µÄµē½ā²ŪÖŠµē½ā£¬Ńō¼«·“Ó¦Ź½ĪŖAg-e-=Ag+”¢Ņõ¼«·“Ó¦Ź½ĪŖ Ag++e-=Ag£¬ĖłŅŌøĆ×°ÖĆŹĒµē¶Ę³Ų£¬
A£®ŅņĪŖČܽāµÄAgŗĶĪö³öµÄAgÖŹĮæĻąµČ£¬ĖłŅŌµē½āÖŹČÜŅŗÅØ¶Č²»±ä£¬ČŌČ»ĪŖ1mol/L£¬¹ŹA“ķĪó£»
B£®½Ļ»īĘĆ½šŹō×÷Ńō¼«£¬Ńō¼«ÉĻ½šŹōŹ§µē×Ó£¬ĖłŅŌŃō¼«·“Ó¦Ź½ĪŖAg-e-=Ag+£¬¹ŹB“ķĪó£»
C£®øł¾ŻAg-e-=Ag+ÖŖ£¬Īö³ö2.16gAgŹ±×ŖŅʵē×ÓŹż=$\frac{2.16g}{108g/mol}$”ĮNA=1.204”Į1022£¬¹ŹCÕżČ·£»
D£®·“Ó¦ÖŠ±»Ńõ»Æn£ØAg£©=$\frac{2.16g}{108g/mol}$=0.02mol£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éµē½āŌĄķ£¬ĪŖøßĘµæ¼µć£¬ÕżČ·ÅŠ¶Ļø÷øöµē¼«ÉĻ·¢ÉśµÄ·“Ó¦ŹĒ½ā±¾Ģā¹Ų¼ü£¬×¢Ņā£ŗ½Ļ»īĘĆ½šŹō×÷Ńō¼«ÉĻ½šŹōŹ§µē×Ó¶ų²»ŹĒµē½āÖŹČÜŅŗÖŠŅõĄė×ÓŹ§µē×Ó£¬ĪŖŅדķµć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šŹōÄĘ“ę·ÅŌŚŹŌ¼ĮĘæÖŠµÄĆŗÓĶĄļ | |
| B£® | “ę·ÅŅŗäåµÄŹŌ¼ĮĘæÖŠÓ¦¼ÓĖ®·ā | |
| C£® | ĻõĖįÓ¦ÓĆ×ŲÉ«ĘæŹ¢×°ĒŅ±Ü¹ā“ę·Å | |
| D£® | ÉÕ¼īÓ¦Ź¢·ÅŌŚ²£Į§ČūµÄÄ„æŚ²£Į§ĘæÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŗĻ³É°±¹¤Ņµ¶Ō¹śĆń¾¼ĆŗĶÉē»į·¢Õ¹¾ßÓŠÖŲŅŖµÄŅāŅ壬ĘäŌĄķŹĒ£ŗN2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H=-92.4KJ/mol£¬
ŗĻ³É°±¹¤Ņµ¶Ō¹śĆń¾¼ĆŗĶÉē»į·¢Õ¹¾ßÓŠÖŲŅŖµÄŅāŅ壬ĘäŌĄķŹĒ£ŗN2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H=-92.4KJ/mol£¬| ²»Ķ¬Ź±¼äø÷ĪļÖŹµÄĪļÖŹµÄĮæ/mol | |||||
| 0min | 1min | 2min | 3min | 4min | |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
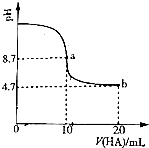
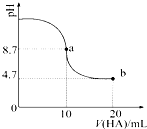 ŹŅĪĀĻĀĻņ10mL 0.1mol•L-1NaOHČÜŅŗÖŠ¼ÓČė0.1mol•L-1µÄŅ»ŌŖĖįHA£¬ČÜŅŗpHµÄ
ŹŅĪĀĻĀĻņ10mL 0.1mol•L-1NaOHČÜŅŗÖŠ¼ÓČė0.1mol•L-1µÄŅ»ŌŖĖįHA£¬ČÜŅŗpHµÄ| A£® | aµćĖłŹ¾ČÜŅŗÖŠc£ØHA£©£¾c£ØA-£© | |
| B£® | aµćĖłŹ¾ČÜŅŗÖŠc£ØNa+£©=c£ØA-£©+c£ØHA£© | |
| C£® | µ±¼ÓČėHAČÜŅŗ10mLŹ±£¬c£ØOH-£©£¼1.0”Į10-7mol•L-1 | |
| D£® | bµćĖłŹ¾ČÜŅŗÖŠc£ØNa+£©£¾c£ØA-£©£¾c£ØH+£©£¾c£ØHA£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ·Šµć/”ę | |
| SiHCl3 | 33.0 |
| SiCl4 | 57.6 |
| HCl | -84 |
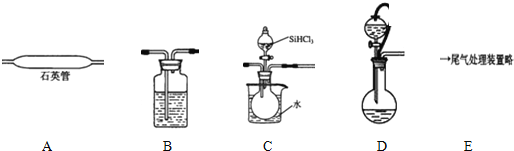
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Ö±šÓėµĪÓŠ·ÓĢŖµÄNaOHČÜŅŗ¹²ČČæÉĒų±šĆŗÓĶÓėÖ²ĪļÓĶ | |
| B£® | Ćŗŗ¬ÓŠ±½”¢¼×±½µČ£¬ĻČøÉĮóŗó·ÖĮó»ńæɵƱ½”¢¼×±½µČ·¼ĻćĢž | |
| C£® | ŌŚĖ®µēĄė³öH+ÅضČĪŖ1”Į10-12mol/LČÜŅŗÖŠŅ»¶Ø“óĮæ“ęŌŚFe2+”¢Na+”¢NO3-”¢Cl- | |
| D£® | ŌŚNH4HSO3ČÜŅŗÖŠ¼ÓČėÉŁĮæNaOHČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖNH4++OH-=NH3•H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | °“ĻµĶ³ĆüĆū·Ø£¬»ÆŗĻĪļ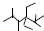 µÄĆū³ĘŹĒ2£¬3£¬5£¬5-Ėļ׻ł-4£¬4-¶žŅŅ»ł¼ŗĶé µÄĆū³ĘŹĒ2£¬3£¬5£¬5-Ėļ׻ł-4£¬4-¶žŅŅ»ł¼ŗĶé | |
| B£® | ÓĆĖįŠŌKMnO4 ČÜŅŗæɼų±š2-¶”Ļ©ŗĶÕż¶”Č© | |
| C£® | ÓĆøŹ°±Ėį[H2N-CH2-COOH]ŗĶ±ū°±Ėį[CH3CH£ØNH2£©COOH]ĖõŗĻ×ī¶ąæÉŠĪ³É3 ÖÖ¶žėÄ | |
| D£® | ŅŅ“¼”¢ŅŅ¶ž“¼”¢±ūČż“¼µÄ·ŠµćŅĄ“ĪÉżøß |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com