
【题目】近年来,乳酸[CH3CH(OH)COOH]成为人们的研究热点之一。乳酸可以用化学方法合成,也可以由淀粉通过生物发酵法制备。请完成下列有关问题:
(1)写出乳酸分子中所有官能团的名称_____________。
(2)在一定条件下,下列物质不能与乳酸发生反应的是________。
A.溴水 B.NaOH溶液 C.Cu(OH)2悬浊液 D.C2H5OH
(3)如果以丙烯(CH2=CH—CH3)为主要原料(其他无机原料任选)合成乳酸,其合成过程的流程图如下:
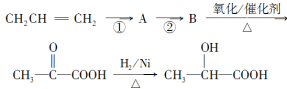
则①的反应类型是________;反应②的化学方程式为____________________________。
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键).
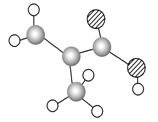
(1)该物质的结构简式为________________.
(2)该物质中所含官能团的名称为______________.
(3)下列物质中,与该产品互为同系物的是(填序号)__________,互为同分异构体的是____________.
①CH3CH===CHCOOH ②CH2===CHCOOCH3 ③CH3CH2CH===CHCOOH
④CH3CH(CH3)COOH ⑤CH2===CHCOOH
(4)该物质在一定条件下发生加聚反应的化学方程式为__________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下可以生成B(C6H12O7)或C(C6H10O8),B和C都不能发生银镜反应。A、B、C都可以被强还原剂还原成为D(C6H14O6)。已知,相关物质被氧化的难易次序是:RCHO最易,R—CH2OH次之,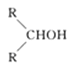 最难。
最难。
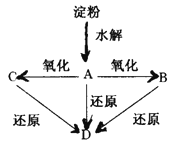
请回答下列问题:
(1)请在下列横线上填写A、B、C、D的结构简式。
A: ;B: ;C: ;D: 。
(2)写出下列反应的化学方程式。
淀粉→A:
A→D:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机高分子化合物甲是一种常用的光敏高分子材料,其结构简式为
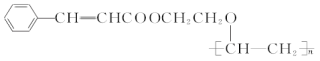 。按如图所示关系可以合成甲,其中试剂I可由乙醇与氧气在催化剂加热条件下反应得到。
。按如图所示关系可以合成甲,其中试剂I可由乙醇与氧气在催化剂加热条件下反应得到。
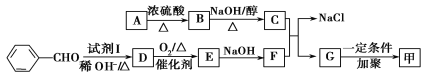
已知:
a.—CH2OH + —CH2OH![]() —CH2OCH2— + H2O
—CH2OCH2— + H2O
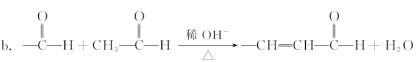
请回答下列问题:
(1)质谱图显示A的相对分子质量是80.5,A分子中氧元素的质量分数为19.88%,碳元素的质量分数为29.81%,其余为氢元素和氯元素,且A的核磁共振氢谱上有三个吸收峰,峰面积之比为2∶2∶1,则A的结构简式为_______________________________________。
(2)试剂I的名称是__________________;B→C的反应类型是__________________。
(3)写出下列反应的化学方程式:
①D→E___________________________________________________________________;
②C+F→G+NaCl_________________________________________________________。
(4)E的一种同分异构体的水解产物有两种,一种能使溴水褪色,另一种在滴加饱和溴水后,有白色沉淀生成,该物质的结构简式为______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂酸异戊酯G(![]() )是一种香料,一种合成路线如下:
)是一种香料,一种合成路线如下:
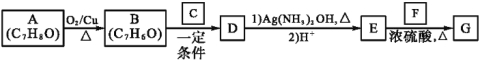
已知以下信息:
①RCHO+R'CH2CHO![]()
![]() ;
;
②C为甲醛的同系物,相同条件下其蒸气与氢气的密度比为22。
回答下列问题:
(1)A的化学名称为 。
(2)B和C反应生成D的化学方程式为 。
(3)F中含有官能团的名称为 。
(4)E和F反应生成G的化学方程式为 ,反应类型为 。
(5)F的同分异构体中不能与金属钠反应生成氢气的共有 种(不考虑立体异构),其中核磁共振氢谱只有两组峰,且峰面积比为3∶1的为 (写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法错误的是( )
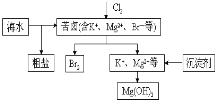
A.向苦卤中通入Cl2是为了提取溴
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物6.4g在氧气中完全燃烧,只生成8.8gCO2和7.2gH2O。下列说法正确的是( )
A. 该化合物仅含碳、氢两种元素
B. 该化合物中碳、氢原子个数比为1:2
C. 无法确定该化合物是否含有氧元素
D. 该化合物中一定含有氧元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4(绿色)、Cr2O72(橙红色)、CrO42(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
(1)Cr3+与Al3+的化学性质相似。在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是_________。
(2)CrO42和Cr2O72在溶液中可相互转化。室温下,初始浓度为1.0 mol![]() L1的Na2CrO4溶液中c(Cr2O72)随c(H+)的变化如图所示。
L1的Na2CrO4溶液中c(Cr2O72)随c(H+)的变化如图所示。

①用离子方程式表示Na2CrO4溶液中的转化反应____________。
②由图可知,溶液酸性增大,CrO42的平衡转化率__________(填“增大”“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为__________。
③升高温度,溶液中CrO42的平衡转化率减小,则该反应的ΔH______0(填“大于”“小于”或“等于”)。
(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl,利用Ag+与CrO42生成砖红色沉淀,指示到达滴定终点。当溶液中Cl恰好沉淀完全(浓度等于1.0×105 mol·L1)时,溶液中c(Ag+)为_______ mol![]() L1,此时溶液中c(CrO42)等于__________ mol
L1,此时溶液中c(CrO42)等于__________ mol![]() L1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×1012和2.0×1010)。
L1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×1012和2.0×1010)。
(4)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O72还原成Cr3+,该反应的离子方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学能在一定的条件下可以转化为电能。
(一)现有如下两个反应:
① 2FeBr2 + 3Cl2 = 2FeCl3+2Br2 ② Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
(1)根据两个反应的本质判断,您认为可以设计成原电池的是 (填反应序号),理由是 。
(二)请根据Fe + CuSO4 = FeSO4 + Cu反应,选择适宜的材料和试剂设计一个原电池
(2)画出原电池装置图,并在图中标注出电极和电解质溶液的名称。
(3)写出该原电池电极反应式:正极: ;负极: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com