
����Ŀ��ijͬѧ����֤̼��Ũ���ᷴӦ��������ʡ����ѽ�װ����ͼ���ӣ���ش��������⡣
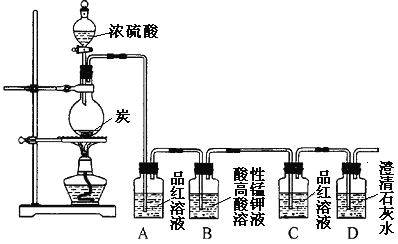
��1����ƿ�з�����Ӧ�Ļ�ѧ��Ӧ����ʽ��___________��
��2��ʵ��������ʹ�õ�Ʒ����Һ����Ŀ�IJ�ͬ��A��ʹ��Ŀ����_____��ͨ��ϴ��ƿC���������___������֤����Ӧ��_______���ѧʽ�����ɡ�
��3��ϴ��ƿB����Һ��ɫ��dz��˵��̼��Ũ���ᷴӦ�IJ���֮һ______�������ƣ�����______�����ʡ�
��4��ʵ����ɺ�ȡ��ϴ��ƿA�е���ɫ��Һ���Թ��У����ȣ��ɹ۲쵽__________��
���𰸡�C+2H2SO4(Ũ)![]() CO2��+2SO2��+2H2O ���鷴Ӧ����SO2�������� ����ʯ��ˮ����� CO2 SO2 ��ԭ�� ��ɫ��Һ�ָֻ���ɫ
CO2��+2SO2��+2H2O ���鷴Ӧ����SO2�������� ����ʯ��ˮ����� CO2 SO2 ��ԭ�� ��ɫ��Һ�ָֻ���ɫ
��������
Ũ�����ǿ�����ԣ������������ܹ���ľ̿����������CO2��SO2��ˮ������Ӧ��Ļ����������ͨ��Aװ�ã�Ʒ����ɫ��˵����SO2�������ɣ�ͨ��B�����Ը��������Һ������SO2�Ļ�ԭ�ԣ���ȥSO2����ͨ��C��Ʒ��ʱ��Ʒ�첻��ɫ��˵��SO2�Ѿ���ȫ��ȥ����ͨ������ʯ��ˮ��ʯ��ˮ����ǣ�˵����CO2�������ɡ�
(1)Ũ�������ǿ�����ԣ��ڼ��ȵ������£��ܰ�ľ̿��������CO2��SO2��ˮ����Ӧ�Ļ�ѧ����ʽΪ��C+2H2SO4(Ũ)![]() CO2��+2SO2��+2H2O��
CO2��+2SO2��+2H2O��
(2)A��Ʒ����ɫ���ɼ��鷴Ӧ����SO2�������ɣ�����Bװ�������Ը��������Һ��ȥSO2��ͨ��ϴ��ƿC��Ʒ�첻��ɫ��D�г���ʯ��ˮ����ǣ�֤����Ӧ��CO2���ɣ�
(3)ϴ��ƿB�����Ը��������Һ��ɫ��dz��˵��̼��Ũ���ᷴӦ�IJ���֮һSO2���л�ԭ�ԣ�
(4)��SO2��Ʒ�������˲��ȶ�����ɫ���ʣ���A��Ʒ����Һ��ɫ���ټ��ȣ���Һ�ָֻ���ɫ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����a��ʾ���淴ӦX��g��+Y��g��Z��g��+M��g�������й�����Z�����ʵ�����ʱ��仯�Ĺ�ϵ����Ҫ�ı���ʼ������ʹ��Ӧ���̰�b���߽��У��ɲ�ȡ�Ĵ�ʩ�ǣ� ��
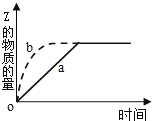
A��ѹ����Ӧ���������
B������һ������Z
C�������¶�
D������X��Ͷ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������㷺����ҩ�ȼ�ϡ����ϵȹ�ҵ������ѧ��ѧʵ�����ﳣ����ͼװ�����Ʊ�����������![]() ���ּг���������ȥ
���ּг���������ȥ![]()
��֪��
�ܶ�(g/cm3) | �۵�(��) | �е�(��) | �ܽ�� | |
�Ҵ� | 0.79 | -114.5 | 78.4 | ��ˮ���� |
���� | 1.05 | 16.6 | 118.1 | ������ˮ���Ҵ� |
�������� | 0.90 | -83.6 | 77.2 | ����ˮ���������Ҵ� |
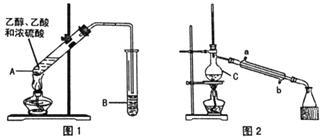
���Ʊ���Ʒ(ͼ1)
��A�м����������Ƭ��������ԭ�����μ���A�У��þƾ��ƻ������ȣ�һ��ʱ�����B�еõ�����������Ʒ��
��1��Ũ���ᡢ�Ҵ�������ļ���˳����___��A�з�����Ӧ�Ļ�ѧ����ʽ��___��
��2��A�����Ƭ��������___�������ܳ��˵����⣬�����е�������___��
��3��B��ʢװ��Һ����___���ռ���������������___��(��ϡ����¡�)��
��.�Ʊ���Ʒ(ͼ2)
��B�е�Һ���Һ��������������Ʒ����һϵ�г��Ӳ�����ת�Ƶ�C�У�����ͼ2װ�ý�һ���������õ�����������Ʒ��
��4��C��������___��
��5��ʵ������У���ȴˮ��___�ڽ���(����ĸ)���ռ���Ʒʱ�����Ƶ��¶�Ӧ��___���ҡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ�У���д��ȷ����
A.��������ˮ��H2O+Cl2=2H++Cl��+ClO��
B.������Ͷ������������Һ�У�2Al+2OH��+2H2O=2AlO2��+H2��
C.��С�մ���ռ�����Һ��ϣ�HCO3��+OH-=H2O+CO32��
D.ʯӢ����NaOH��Һ��Si4++2O2��+2OH��=SiO32��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С���Ա���ϩ����ϩΪ��Ҫԭ�ϣ���Ƴ�ҽҩ�м���G�ĺϳ�·����ͼ��
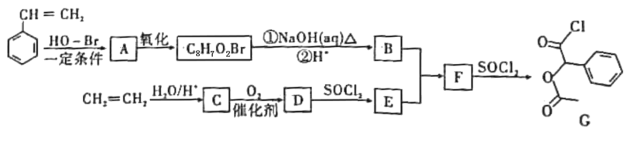
��֪RCOOH![]() RCOCl
RCOCl![]() RCOOR����
RCOOR����
��1��B�к��������ŵ�����Ϊ___��D�Ľṹ��ʽΪ___��
��2����ϩ��ij��ͬϵ��Ļ�ѧ����Ϊ������ϩ���������ϩ�Ľṹ��ʽΪ___��
��3��B��ͨ�����Ӽ���ˮ�����л���X��X���������ϣ���ṹ�к���������Ԫ��״�ṹ����Bת��ΪX�Ļ�ѧ����ʽ��___��
��4��M��G��ͬ���칹�壬�������нṹ�����ʵķ����廯����M����___�֣������������칹����
��1molM��������Һ��Ӧ����ܵ�4molAg��
�ڱ��������ĸ�ȡ�����������λ��Ϊ![]() ��
��
�ۺ˴Ź�������Ϊ5��壬�ҷ����Ϊ2��2��2��2��1��
��M�ܷ�����ȥ��Ӧ��
д��M������ȥ��Ӧ�Ļ�ѧ����ʽ��___��һ�����ɣ���
��5����Ƴ��Լױ�Ϊԭ���Ʊ�B�ĺϳ�·�ߣ����Լ���ѡ����֪��RCHO![]()
![]() ��RCN
��RCN![]() RCOOH��___��
RCOOH��___��
�ϳ�·�߳��õı�ʾ��ʽΪ��A![]() B����
B����![]() Ŀ����
Ŀ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�� M�������ճ�������һ����Ҫ���ϣ�Ҳ��һ����Ҫ�Ļ���ԭ�ϣ�������ʱ����ɫ��Ӧ�ʻ�ɫ��A��B��D��Ϊ���ʣ���F����Һ�м������軯����Һ����Һ���Ѫ��ɫ�������ʵ�ת����ϵ����ͼ��ʾ��

����������Ϣ�ش��������⣺
��1��M��ˮ�������Ļ�ѧ����ʽ____________��
��2��д��E����ˮ�ĵ��뷽��ʽ__________��
��3��F��D��Ӧ����G�����ӷ���ʽΪ____________��
��4����G����Һ�еμ�C����Һ���۲쵽������Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������NO��O2���ɣ���֪��2L�ܱ������ڣ�800��ʱ��Ӧ��2NO(g)��O2(g)![]() 2NO2(g) ��H��n(NO)��n(O2)��ʱ��ı仯�����
2NO2(g) ��H��n(NO)��n(O2)��ʱ��ı仯�����
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.200 | 0.100 | 0.080 | 0.050 | 0.050 | 0.050 |
n(O2)/mol | 0.100 | 0.050 | 0.040 | 0.025 | 0.025 | 0.025 |
��1����֪��K800��>K1000������÷�Ӧ����H___0(��������������С����)����O2��ʾ0��2 s�ڸ÷�Ӧ��ƽ������Ϊ___��
��2����˵���÷�Ӧ�Ѵﵽƽ��״̬����___��
a��������������ɫ���ֲ��� b��2v��(NO)��v��(O2)
c��������ѹǿ���ֲ��� d�������������ܶȱ��ֲ���
��3��Ϊʹ�÷�Ӧ�������������NO��ת���ʣ���ƽ��������Ӧ�����ƶ���Ӧ��ȡ�Ĵ�ʩ��_____��
��4�������������£�����ͨ��2molNO��1molO2��ƽ�ⳣ��K��___��
��5�������������£�����ʼͨ�����0.2molNO2���壬�ﵽ��ѧƽ��ʱ��NO2��ת����Ϊ__��
��6��úȼ�ղ����������������������CH4����ԭNOx�������������������Ⱦ��
��CH4(g)��4NO(g)![]() 2N2(g)��CO2(g)��2H2O ��H<0
2N2(g)��CO2(g)��2H2O ��H<0
��CH4(g)��2NO2(g)![]() N2(g)��CO2(g)��2H2O(g) ��H<0
N2(g)��CO2(g)��2H2O(g) ��H<0
���ڷ�Ӧ�ڣ������NO2��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��____��
a������ԭ�����ı���� b�������¶� c����СͶ�ϱ�[n(NO2)/n(CH4)] d������ѹǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������辧�����������״�ṹ���侧��ṹģ����ͼ��������۲��ģ�ͺ�ش��������⣺
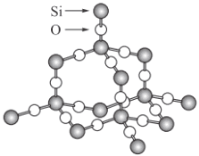
(1)�������辧������С������______��ԭ�ӣ�����ṹ�д�����__________ԭ��Ϊ���ġ�________ԭ��Ϊ�������������ṹ��
(2)�����д��ڵ���������________��
A�����ۼ���B�����Ӽ���C����λ����D�����»�����E�����
(3)����LawreceLiremore����ʵ����(LLNL)��V.Lota.C.S.Yoo��Cynn�ɹ����ڸ�ѹ�½�CO2ת��Ϊ��������SiO2�ṹ��ԭ�Ӿ��壬���й���CO2��ԭ�Ӿ���˵����ȷ����________��
A��CO2��ԭ�Ӿ���ͷ��Ӿ��廥Ϊͬ��������
B����һ�������£�CO2ԭ�Ӿ���ת��Ϊ���Ӿ����������仯
C��CO2��ԭ�Ӿ����CO2�ķ��Ӿ��������ͬ����������
D����CO2��ԭ�Ӿ����У�ÿ��Cԭ�ӽ��4��Oԭ�ӣ�ÿ��Oԭ�ӽ������Cԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ԭCO2�ǽ������ЧӦ����Դ�������Ҫ�ֶ�֮һ���о���������Cu/ZnO���������£�CO2��H2�ɷ�������ƽ�з�Ӧ���ֱ�����CH3OH��CO����Ӧ���Ȼ�ѧ����ʽ���£�
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H1=-53.7kJ��mol-1 I
CH3OH(g)+H2O(g) ��H1=-53.7kJ��mol-1 I
CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H2 II
CO(g)+H2O(g) ��H2 II
ijʵ���ҿ���CO2��H2��ʼͶ�ϱ�Ϊ1��2.2������ͬѹǿ�£�������ͬ��Ӧʱ��������ʵ�����ݣ�
T(K) | ���� | CO2ת���ʣ�%�� | �״�ѡ���ԣ�%�� |
543 | Cat.1 | 12.3 | 42.3 |
543 | Cat.2 | 10.9 | 72.7 |
553 | Cat.1 | 15.3 | 39.1 |
553 | Cat.2 | 12.0 | 71.6 |
����ע��Cat.1��Cu/ZnO���װ���Cat.2��Cu/ZnO����Ƭ���״�ѡ���ԣ�ת����CO2�����ɼ״��İٷֱ�
��֪����CO��H2�ı�ȼ���ȷֱ�Ϊ-283.0kJ��mol-1��-285.8kJ��mol-1
��H2O(l)=H2O(g) ��H3=44.0kJ��mol-1
��ش𣨲������¶ȶ���H��Ӱ�죩��
(1)��ӦI��ƽ�ⳣ������ʽK=___��
(2)���������CO2ת��ΪCH3OHƽ��ת���ʵĴ�ʩ��___��
A��ʹ�ô���Cat.1
B��ʹ�ô���Cat.2
C�����ͷ�Ӧ�¶�
D��Ͷ�ϱȲ��䣬���ӷ�Ӧ���Ũ��
E������CO2��H2�ij�ʼͶ�ϱ�
(3)����ʵ�����ݱ���������ͬ�¶��²�ͬ�Ĵ�����CO2ת����CH3OH��ѡ������������Ӱ�죬��ԭ����___��
(4)��ͼ�зֱ���ӦI����������Cat.1����Cat.2��������¡���Ӧ���̡�������ʾ��ͼ___��

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com