
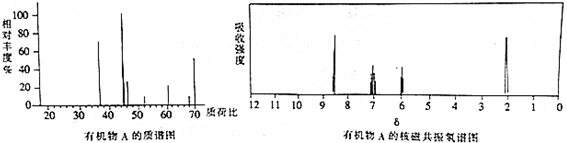
·ÖĪö £Ø1£©øł¾ŻÖŹĘ×Ķ¼ÖŠŹż¾ŻÅŠ¶ĻøĆÓŠ»śĪļµÄĻą¶Ō·Ö×ÓĮ棻
£Ø2£©·Ö×ÓÖŠÓŠ¼øÖÖĄąŠĶµÄĒāŌ×Ó¾Ķ»į³öĻÖ¼øøö·å£»
£Ø3£©ŗģĶā¹āĘ×±ķÕ÷µ½CØTCŗĶCØTOµÄ“ęŌŚ£¬Ļą¶Ō·Ö×ÓÖŹĮæĪŖ70£¬·Ö×ÓÖŠŗ¬ÓŠ1øöCØTCŗĶ1øöCØTO£¬Č„µō1øöCØTCŗĶ1øöCØTOµÄŹ½ĮæŗóŹ£ÓąŹ½ĮæĪŖ70-24-28=18£¬Ó¦ŗ¬ÓŠ1øöCŌ×Ó”¢6øöHŌ×Ó£¬¹ŹøĆÓŠ»śĪļ·Ö×ÓŹ½ĪŖC4H6O£¬ŗĖ“Ź²ÕńĒāĘ×Ķ¼·åµÄĒæ¶Č±ČĪŖ2£ŗ1£ŗ1£ŗ2£¬ŌņÓŠ4ÖÖHŌ×Ó£¬×īŗóČ·¶Ø½į¹¹¼ņŹ½£®
½ā“š ½ā£ŗ£Ø1£©øł¾ŻÖŹĘ×Ķ¼æÉÖŖ£¬øĆÓŠ»śĪļµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ70£»
¹Ź“š°øĪŖ£ŗ70£»
£Ø2£©·Ö×ÓÖŠ¹²ÓŠ4øö·å£¬ĖłŅŌÓŠ4ÖÖ»Æѧ»·¾³²»Ķ¬µÄĒāŌ×Ó£»
¹Ź“š°øĪŖ£ŗ4£»
£Ø3£©ŗģĶā¹āĘ×±ķÕ÷µ½CØTCŗĶCØTOµÄ“ęŌŚ£¬Ļą¶Ō·Ö×ÓÖŹĮæĪŖ70£¬·Ö×ÓÖŠŗ¬ÓŠ1øöCØTCŗĶ1øöCØTO£¬Č„µō1øöCØTCŗĶ1øöCØTOµÄŹ½ĮæŗóŹ£ÓąŹ½ĮæĪŖ70-24-28=18£¬Ó¦ŗ¬ÓŠ1øöCŌ×Ó”¢6øöHŌ×Ó£¬¹ŹøĆÓŠ»śĪļ·Ö×ÓŹ½ĪŖC4H6O£¬ŗĖ“Ź²ÕńĒāĘ×Ķ¼·åµÄĒæ¶Č±ČĪŖ2£ŗ1£ŗ1£ŗ2£¬²»Ķ¬HŌ×ÓŹżÄæ·Ö±šĪŖ2£ŗ1£ŗ1£ŗ2£¬øĆÓŠ»śĪļ½į¹¹¼ņŹ½ĪŖ£ŗH2C=CHCH2CHO£»
¹Ź“š°øĪŖ£ŗC4H6O£»H2C=CHCH2CHO£»
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļ½į¹¹µÄĶʶĻ”¢ŗĖ“Ź²ÕńĒāĘ×”¢ŗģĶā¹āĘ×µČ£¬²ąÖŲæ¼²éѧɜ·ÖĪöĶĘĄķÄÜĮ¦£¬£Ø3£©ÖŠ×¢ŅāĄūÓĆ²ŠÓą·Ø½ųŠŠ·Ö×ÓŹ½Č·¶Ø£¬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
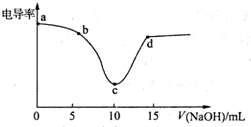 ĄūÓƵēµ¼ĀŹ“«øŠĘ÷æÉ»ęÖʵēµ¼ĀŹĒśĻßĶ¼£¬ĻĀĶ¼ĪŖÓĆ0.1mol•L-1NaOHČÜŅŗµĪ¶Ø10mL£¬0.1mol•L-1ŃĪĖį¹ż³ĢÖŠµÄµēµ¼ĀŹĒśĻߣ®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©
ĄūÓƵēµ¼ĀŹ“«øŠĘ÷æÉ»ęÖʵēµ¼ĀŹĒśĻßĶ¼£¬ĻĀĶ¼ĪŖÓĆ0.1mol•L-1NaOHČÜŅŗµĪ¶Ø10mL£¬0.1mol•L-1ŃĪĖį¹ż³ĢÖŠµÄµēµ¼ĀŹĒśĻߣ®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©| A£® | µēµ¼ĀŹ“«øŠĘ÷ÄÜÓĆÓŚÅŠ¶ĻĖį¼īÖŠŗĶµĪ¶ØµÄÖÕµć | |
| B£® | øĆ¹ż³ĢÖŠ£¬aµćĖłŹ¾ČÜŅŗµÄµ¼µēŠŌ×īĒæ | |
| C£® | cµćµēµ¼ĀŹ×īŠ”ŹĒŅņĪŖ“ĖŹ±ČÜŅŗÖŠµ¼µēĪ¢Į£µÄŹżÄæ×īÉŁ | |
| D£® | dµćĖłŹ¾ČÜŅŗÖŠ“ęŌŚ£ŗc£ØCl-£©+c£ØOH-£©=c£ØH+£©+c£ØNa+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ÅØĻõĖįÓė×ćĮæĶʬ·“Ó¦Ź±£¬ĻČÉś³Éŗģ×ŲÉ«ĘųĢ壬ŗóÉś³ÉĪŽÉ«ĘųĢå | |
| B£® | ÅØĮņĖį¾ßÓŠĒæŃõ»ÆŠŌ£¬³£ĪĀĻĀæɽ«ĀĮµÄµ„ÖŹŃõ»Æ£¬Ņņ“Ė£¬²»ÄÜÓĆĀĮ¹Ž³µŌĖŹäÅØĮņĖį | |
| C£® | ±„ŗĶĀČĖ®¼ČÓŠĖįŠŌÓÖÓŠĘư׊Ō£¬¼ÓČėNaHCO₃ŗóĘư׊Ō¼õČõ | |
| D£® | ÅØŃĪĖįÓė×ćĮ涞Ńõ»ÆĆĢ·“Ó¦ŗó£¬ŃĪĖįÓŠŹ£Óą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 4£ŗ5£ŗ2 | B£® | 2£ŗ5£ŗ4 | C£® | 1£ŗ3£ŗ2 | D£® | 3£ŗ2£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū¢Ż | B£® | ¢Ł¢Ś¢Ū¢Ü¢Ż | C£® | ¢Ł¢Ū¢Ż | D£® | ¢Ś¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1.5mol NaCl | B£® | 0.5mol H2SO4 | C£® | 0.6mol H2O2 | D£® | 1mol HNO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com