
�⼰�仯�����ںϳ�ɱ������ҩ��ȷ�����й㷺��;���ش��������⣺
��1�������ĵ⸻���ں����У���ˮ��ȡ��Ũ��������Ũ��Һ�м�MnO2��H2SO4�����ɵõ�I2���÷�Ӧ�Ļ�ԭ����Ϊ____________��
��2������Ũ��Һ�к���I-��Cl-�����ӣ�ȡһ������Ũ��Һ�������еμ�AgNO3��Һ����AgCl��ʼ����ʱ����Һ��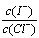 Ϊ��_____________����֪Ksp��AgCl��=1.8��10-10��Ksp��AgI��=8.5��10-17��
Ϊ��_____________����֪Ksp��AgCl��=1.8��10-10��Ksp��AgI��=8.5��10-17��
��3����֪��Ӧ2HI(g) ===H2(g) + I2(g)�Ħ�H= +11kJ��mol��1��1mol H2(g)��1mol I2(g)�����л�ѧ������ʱ�ֱ���Ҫ����436kJ��151kJ����������1molHI(g)�����л�ѧ������ʱ�����յ�����Ϊ______________kJ��
��4��Bodensteins�о������з�Ӧ��
2HI(g) H2(g) + I2(g)
H2(g) + I2(g)
��716Kʱ�����������е⻯������ʵ�������x(HI)�뷴Ӧʱ��t�Ĺ�ϵ���±���
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0. | 0.773 | 0.780 | 0.784 |
�� ��������ʵ�������÷�Ӧ��ƽ�ⳣ��K�ļ���ʽΪ��___________��
�� ������Ӧ�У�����Ӧ����Ϊv��= k����x2(HI)���淴Ӧ����Ϊv��=k����x(H2)��x(I2)������k����k��Ϊ���ʳ�������k��Ϊ________(��K��k����ʾ)����k�� = 0.0027min-1����t=40minʱ��v��=__________min-1
�� ������ʵ�����ݼ���õ�v��~x(HI)��v��~x(H2)�Ĺ�ϵ������ͼ��ʾ�������ߵ�ijһ�¶�ʱ����Ӧ���´ﵽƽ�⣬��Ӧ�ĵ�ֱ�Ϊ_________________������ĸ��

���𰸡���1��MnSO4��
��2�� 4.7��10-7��
��3�� 299
��4����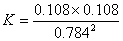 ����k��= k��/K ��1.95��10-3���� A��E
����k��= k��/K ��1.95��10-3���� A��E
����������1�����и���������ԭ��Ӧ����ʽ���жϻ�ԭ��������ѧ���濼����Ǩ��ʵ������������ԭ���ɵ�MnSO4��
��2�� ��ϵ�м����Ȼ������е⻯��ʱ�����ڳ���ת��ƽ�⣺AgI(s) +Cl�� AgCl(s) +I����
AgCl(s) +I����
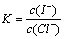
���ӡ���ĸͬʱ����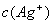 ���У�
���У�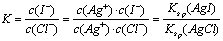 ����Ksp��AgCl��=1.8��10-10��Ksp��AgI��=8.5��10-17����ã�
����Ksp��AgCl��=1.8��10-10��Ksp��AgI��=8.5��10-17����ã�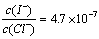 ��
��
��3�� ����һ��ȡ��ֵ�����㣬��H=E����Ӧ������ܺͣ���E������������ܺͣ�����1molHI��g�������л�ѧ������ʱ�����յ�����ΪxkJ��������㣺+11=2x����436+151��
x =299
��4�� �����еķ�Ӧ�DZȽ�����ģ���Ӧǰ�����������ȣ���ͬ����ʼ̬�����״ﵽ��Ч��ƽ��״̬�����ע������е����������������������������ݡ�
716Kʱ��ȡ��һ�����ݼ��㣺2HI��g�� H2��g��+I2��g��
H2��g��+I2��g��
n��ʼ����ȡ1mol�� 1 0 0
��n ��0.216�� ��0.108�� ��0.108��
n��ƽ�� 0.784 ��0.108�� ��0.108��
��ѧƽ�ⳣ��Ϊ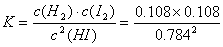
��С���״��㣺����ʽ�ᱻ����Ϊ�DZ���ʽ��
���ʵ�Ҫ���ǣ�ƽ��״̬�£�v��= v�������У�k����x2(HI) = k����x(H2)��x(I2)
����k��/ k��=�� x(H2)��x(I2)��/ x2(HI)=K
���� k��= k��/K
�� �ʿ��ƺ��ѣ���ʵע����µ�����ЧӦ���ӿ컯ѧ��Ӧ���ʡ�ʹƽ���ƶ�������ͻ�ƣ��ȿ�ͼ���Ұ���������Ӧ�����ʼӿ죬���������ƣ�ƽ�⣨������֪����Ӧ���ȣ������ƶ����� �������ơ���ǰ�������ҳ�A�㡣ͬ�����ҳ�E�㡣
�������ơ���ǰ�������ҳ�A�㡣ͬ�����ҳ�E�㡣
�����㶨λ����ѧƽ�ⳣ�����㣻��ѧƽ��֪ʶ���ۺ����ã��������ڸ���ƽ��֪ʶ���ۺ����ã������Ѷ�Ϊ���ѵȼ���
����ʦ���硿����ƫ�ѡ�ǰ��С�����dz��濼�㣬�Ѷ�Ϊһ��ȼ������һС�⸳��10�֣��Ѷ�ƫ�����������������龰����4���ʢ�С���������ö����Dz��֣��ؼ���Ҫ�ǵ�ƽ���־֮һ����v��= v�����ҵ�k����k����K����ϵ����ͻ�ơ���4���ʢ�С�ʵ�ͼ��Ҫ�ܿ���ʶ������������淴Ӧ������x(H2)�ı仯���ұ�����������Ӧ������x(HI)�ı仯����ϸ������ͼ�������ѱ���v����v��������Ҳ�ɰ������ķ�������������Ȼ������������ǹ��õģ������������ߺ�����ĺ����Dz�ͬ�ġ�����ƽ���ƶ����º�����仯ʱһ��Ҫע����һ�㡣


 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij����һԪȩ����������Ӧʱ������21.6 g��������������ȩ��ȫȼ�գ�����CO2�����Ϊ13.44 L(��״��)���� ��ȩ��(����)
��ȩ��(����)
A����ȩ B����ȩ C����ȩ D��3����ȩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ȷ��ȡ20.00mLij����HCl��Һ����ƿ�У���0.1000mol��L-1NaOH��Һ�ζ�������˵����ȷ���ǣ� ��
A���ζ���������ˮϴ�Ӻ�װ��NaOH��Һ���еζ�
B������NaOH��Һ���룬��ƿ����ҺpH��С���
C���÷�̪��ָʾ��������ƿ����Һ�ɺ�ɫ����ɫʱֹͣ�ζ�
D���ζ����յ�ʱ�����ֵζ��ܼ��첿�������Σ���ⶨ���ƫС
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������Ϊ1��0L���������ܱ������м�����������ͬ��̼�ۣ��ٷֱ����0.1molCO2��0.2molCO2���ڲ�ͬ�¶��·�ӦCO2(g)��c(s)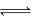 2CO(g)�ﵽƽ�⣬ƽ��ʱCO2�����ʵ���Ũ��c(CO2)
2CO(g)�ﵽƽ�⣬ƽ��ʱCO2�����ʵ���Ũ��c(CO2)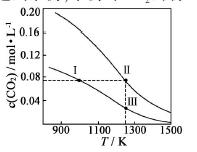 ���¶ȵı仯��ͼ��ʾ(ͼ�Т�������������)������˵����ȷ���ǣ� ��
���¶ȵı仯��ͼ��ʾ(ͼ�Т�������������)������˵����ȷ���ǣ� ��
A����ӦCO2(g)��c(s)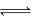 2CO(g) ��S>0����H<0
2CO(g) ��S>0����H<0
B����ϵ����ѹǿP�ܣ�P��(״̬��)>2P�ܣ�״̬��
C����ϵ��c(CO)��c(CO��״̬��)<2c(CO��״̬��)
D���淴Ӧ����V�棺V�棨״̬��>V�棨״̬��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��O2��HClת��ΪCl2�������Ч�棬������Ⱦ��
��1����ͳ�ϸ�ת��ͨ������ͼ��ʾ�Ĵ���ѭ��ʵ�֣�

���У���Ӧ��Ϊ��2HCl(g) + CuO(s) 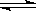 H2O(g)+CuCl2(g) ��H1
H2O(g)+CuCl2(g) ��H1
��Ӧ������1molCl2(g)�ķ�Ӧ��Ϊ��H2�����ܷ�Ӧ���Ȼ�ѧ����ʽΪ , (��Ӧ���á�H1�͡�H2��ʾ)��
��2������RuO2����������HClת��ΪCl2���ܷ�Ӧ���и��õĴ����ԣ�
��ʵ������һ��ѹǿ�£��ܷ�Ӧ��HClƽ��ת�������¶ȱ仯��aHCl��T������ͼ12�����ܷ�Ӧ�ġ�H 0 ,�����������������������A��B�����ƽ�ⳣ��K(A)��K(B)�нϴ���� ��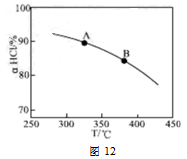
��������ʵ������ѹ�����ʹѹǿ��������ӦaHCl��T���ߵ�ʾ��ͼ������Ҫ˵�����ɣ� ��
�����д�ʩ�����������aHCl����  ��
��
A������n(HCl) B������n(O2) C��ʹ�ø��õĴ��� D����ȥH2O
��3��һ�������²�÷�Ӧ������n(Cl2)���������£�
| t(min) | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| n(Cl2)/10-3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
����2.0��6.0min����HCl�����ʵ����仯��ʾ�ķ�Ӧ���ʣ���mol��min-1Ϊ��λ��д��������̣���
��4��Cl2��;�㷺��д����Cl2�Ʊ�Ư�۵Ļ�ѧ����ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȷ���ǣ���
| A�� | Na2O��Na2O2���ܺ�ˮ��Ӧ���ɼ�����Ǽ��������� | |
| B�� | Na2CO3��Һ��NaHCO3��Һ���ܸ�CaCl2��Һ��Ӧ�õ���ɫ���� | |
| C�� | Na2O2Ӧ�������ܷ⡢������������Ĺ��ƿ�� | |
| D�� | Na2O2��������������Na2O���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ��ij��ȤС����ݿα�ʵ����Ƶ�һ����˵��̼������̼���������ȶ��� ����ʵ�飮��۲���ͼʵ��װ�á�����ʵ��ԭ�������ж�����˵�������������в���ѧ���ǣ���
����ʵ�飮��۲���ͼʵ��װ�á�����ʵ��ԭ�������ж�����˵�������������в���ѧ���ǣ���
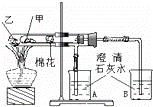
| A�� | ��ΪС�մ���Ϊ���� | |
| B�� | ����ʵ�������û�з���A�ձ��ij���ʯ��ˮ����� | |
| C�� | ���Ȳ��þ��ܿ���A�ձ��ij���ʯ��ˮ����� | |
| D�� | Ҫ֤��̼�����������ܲ���ˮ������С�Թ�������մ����ˮ����ͭ��ĩ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪���ȼ��a g��Ȳ����ʱ����1 mol������̼�����Һ̬ˮ�����ų�����b kJ������Ȳȼ�յ��Ȼ�ѧ����ʽ��ȷ����(����)
A��2C2H2(g)��5O2(g)===4CO2(g)��2H2O(l) ��H����4b kJ��mol��1
B��C2H2(g)��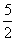 O2(g)===2CO2(g)��H2O(l) ��H����2b kJ��mol��1
O2(g)===2CO2(g)��H2O(l) ��H����2b kJ��mol��1
C��2C2H2(g)��5O2(g)===4CO2(g)��2H2O(l) ��H����2b kJ��mol��1
D��2C2H2(g)��5O2(g)===4CO2(g)��2H2O(l) ��H����b kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�л���A��ũҩ�����е�һ���м��壬�ṹ��ʽ����ͼ��ʾ��������������ȷ����(����)
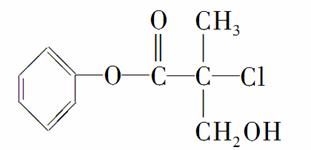
A��1 mol A�������4 mol H2�����ӳɷ�Ӧ
B���л���A������һ����������HBr������Ӧ
C���л���A��Ũ�����ϼ��ȣ����Է�����ȥ��Ӧ
D��1 mol A��������NaOH��Һ��Ӧ������������2 mol NaOH
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com