
 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:选择题
 pH=2的X、Y、Z三种酸的溶液各1mL,分别稀释到1000mL,其pH与溶液体积(V)的变化关系如图所示,下列正确的是 ( )
pH=2的X、Y、Z三种酸的溶液各1mL,分别稀释到1000mL,其pH与溶液体积(V)的变化关系如图所示,下列正确的是 ( )| A. | X、Y和Z都是弱酸 | B. | 稀释前的浓度大小为c(Z)>c(X)>c(Y) | ||
| C. | 稀释前电离程度大小为X>Y>Z | D. | pH=2时,X、Y、Z都是稀溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,铁比铝更易生锈,说明铁比铝活泼 | |
| B. | 钠比铜活泼,将钠投入硫酸铜溶液中,会有红色的铜析出 | |
| C. | 镁粉中混有的少量铝粉,可加足量NaOH溶液过滤除去 | |
| D. | 从1L 0.5mol/L FeCl3溶液中取出100mL,其中Cl-浓度为0.15 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NA个氢气分子所占的体积为22.4L | |
| B. | 常温下,22.4 L NO2中所含的氧原子数为2 NA | |
| C. | 14 g氮气所含的N原子数为NA | |
| D. | 标准状况下,22.4 L水所含的H2O分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol/L NH4Cl溶液 | B. | 0.5mol/L盐酸 | ||
| C. | 0.5mol/LH2SO4 | D. | 0.5mol/L醋酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 地沟油属于混合物,石蜡油属于纯净物 | |
| B. | 地沟油属于酯类,石蜡油属于烃类 | |
| C. | 地沟油可以用来制肥皂,石蜡油是石油裂解的产品 | |
| D. | 地沟油属于高分子化合物,石蜡油属于小分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
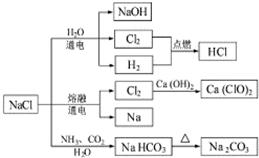 NaCl是常用的食品调味剂,也是一种化工原料,可以制备一系列物质.下列说法正确的是( )
NaCl是常用的食品调味剂,也是一种化工原料,可以制备一系列物质.下列说法正确的是( )| A. | 25℃时,NaHCO3在水中的溶解度比Na2CO3的小 | |
| B. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 | |
| C. | 常温下液氯能用钢瓶贮存,所以Cl2不与铁反应 | |
| D. | 图中所示转化反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com