
| A��Q1+Q2��Q3 |
| B���μӷ�Ӧ��H2��Cl2����������������HCl�������� |
| C��Q1+Q2��2Q3 |
| D���μӷ�Ӧ��H2��Cl2������С��������HCl�������� |


 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1mol��13% |
| B��0.1mol��26% |
| C��0.2mol��26% |
| D��0.2mol��74% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ӧ���ʿ����ں�����ѧ��Ӧ�Ŀ��� |
| B��������Ӧ���ʵ���Ҫ�������¶Ⱥ�ѹǿ |
| C�����淴Ӧ�ﵽ��ѧƽ��ʱ�������淴Ӧ��������Ҳ�Ϊ�� |
| D������Ӧ��Ũ�ȣ���߷�Ӧ���¶ȶ�������Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��a��b��c��d���� |
| B��ֻ��a��d |
| C��һ����d��������c |
| D����c��d |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A��ʯī�ͽ��ʯ��Ϊͬ���칹�壬�֮���ת���ǻ�ѧ�仯 |
| B��C��s��ʯī���TC��s�����ʯ����H=-1.9 kJ?mol-1 |
| C�����ʯӲ�ȴ���ʯī�������ʯ���ȶ�������ʯī |
| D��1 molʯī���ܼ��ܱ�1 mol���ʯ���ܼ���С1.9 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������һ�����ԣ��������������ͷ����� |
| B�������Ż������������������찲ȫ��� |
| C����֬�������ɵĸ�֬�������Ƿ�������Ч�ɷ� |
| D����ʳ��ȥ��ˮ���е�ˮ��ʱ����������ˮ�ⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����Ƶ���ˮ�ڹ�����������ɫ��dz |
| B������ƿ�Ǻ��д��������ݳ� |
| C����֪2HI��g��?H2��g��+I2��g�������ݻ��ɱ���ܱ��������Ѵ�ƽ���HI��I2��H2����������ѹ�������������ɫ���� |
| D����ҵ���õ����������ϳɰ����Ĺ����У�ͨ����ѹ������Һ��������ת���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
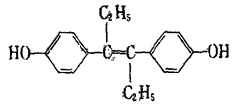
| A�����������л��ܼ� |
| B��1mol���л����������NaOH��Na2CO3�����ʵ�����Ϊ2mol |
| C��1mol���л��������5mol Br2������Ӧ |
| D�����л�������У������14��̼ԭ�ӹ�ƽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���� | B���� | C���� | D���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com