
 ��ͼʾ��װ�ý��е�⣬ͨ��һ��ʱ�����Pt�缫��������ð����
��ͼʾ��װ�ý��е�⣬ͨ��һ��ʱ�����Pt�缫��������ð�������� ��pt�缫��������ð����֪PtΪ������������������EΪ������FΪ������A��FeΪ������B��ͭΪ������A�صĵ缫��Ӧ�ֱ��ǣ������缫��Ӧ����ߣ���Ag++e-��Ag�������缫��Ӧ���ұߣ���4OH--4e-��2H2O+O2����B�صĵ缫��Ӧ�ֱ��ǣ������缫��Ӧ����ߣ���2H++2e-=H2���������缫��Ӧ���ұߣ���Cu-2e-=Cu2+����ϵ缫����ʽ�����⣮
��� �⣺��pt�缫��������ð����֪PtΪ������������������EΪ������FΪ������A��FeΪ������B��ͭΪ������A�صĵ缫��Ӧ�ֱ��ǣ������缫��Ӧ����ߣ���Ag++e-��Ag�������缫��Ӧ���ұߣ���4OH--4e-��2H2O+O2����B�صĵ缫��Ӧ�ֱ��ǣ������缫��Ӧ����ߣ���2H++2e-=H2���������缫��Ӧ���ұߣ���Cu-2e-=Cu2+��
��1���ɷ�����֪��FΪ������B��ͭΪ����������������Cu2+���缫����ʽΪCu-2e-=Cu2+��
�ʴ�Ϊ������Cu-2e-=Cu2+��
��2��A�صĵ缫��Ӧ�ֱ��ǣ������缫��Ӧ����ߣ���Ag++e-��Ag�������缫��Ӧ���ұߣ���4OH-��2H2O+O2��+4e-
�ܷ�Ӧ��4AgNO3+2H2O$\frac{\underline{\;���\;}}{\;}$4Ag+O2��+4HNO3�����ӷ���ʽ��4Ag++2H2O$\frac{\underline{\;ͨ��\;}}{\;}$4Ag+O2��+4H+��
�ʴ�Ϊ��4Ag++2H2O$\frac{\underline{\;ͨ��\;}}{\;}$4Ag+O2��+4H+��
��3��A��Fe������Pt������
�ʴ�Ϊ����������
��4��B����ʯīΪ�����������������ӵõ��ӣ���缫��ӦΪ2H++2e-=H2����
�ʴ�Ϊ��2H++2e-=H2����
���� �����ۺϿ������֪ʶ��������ѧ���ķ��������������Ŀ��飬ע�����ԭ��ء����صĹ���ԭ���Լ��缫����ⷽ��ʽ����д����Ϸ�Ӧ�ķ���ʽ���㣬�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
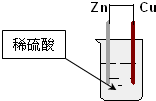
| A�� | ͭƬ���������ݲ��� | B�� | ������ӦΪ��Cu-2e-=Cu2+ | ||
| C�� | пΪ������ͭΪ���� | D�� | ����ͨ��пƬ����������ͭƬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���������mL�� | 5 | 15 | 20 | 50 | x | 120 | 150 |
| ����CO2�����mL�� | 0 | 224 | 448 | 1792 | 4480 | 4480 | 4480 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڱ�״���£�1molˮ��1molH2�������Լ��22.4L | |
| B�� | 2gH2��44gCO2�������� | |
| C�� | 1molij��������Ϊ22.4L���������һ�����ڱ�״�� | |
| D�� | �ڱ�״���£�1gH2��11.2LO2�����ʵ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ʵ����ձ��þƾ�ϴ�� | |
| B�� | ����������Ӧʵ����Թ���ϡ����ϴ�� | |
| C�� | �����ͷ��ڴ���Ƥ���IJ���ƿ�� | |
| D�� | ��˫��ˮ�е��뼸�����Ȼ�����Һ�ӿ�ֽ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ����� | c��NH4Cl��/mol��L-1 | �¶�/�� | ���������� | ʵ��Ŀ�� |
| �� | 0.5 | 30 | x | - |
| �� | 1.5 | i | y | ̽��Ũ�ȶ��Ȼ��ˮ��ƽ���Ӱ�� |
| �� | 0.5 | 35 | z | ii |
| �� | 2.0 | 40 | m | ̽���¶ȡ�Ũ��ͬʱ���Ȼ��ˮ��ƽ���Ӱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �٢ڢ� | C�� | �ۢ� | D�� | �٢� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com