
| A. | 0.05 mol•L-1 的 H2SO4 溶液 pH=1 | |
| B. | 0.001 mol•L-1 的 NaOH 溶液 pH=ll | |
| C. | 0.005 mol•L-1的H2SO4溶液与0.01 mol•L-1的NaOH溶液等体积混合,混合后溶液pH为5,溶液显酸性 | |
| D. | 完全中和pH=3的H2SO4溶液50 mL,需要PH=11的NaOH溶液50mL |
分析 100℃的温度下,水的离子积KW=1×10-12,所以该温度下的中性溶液中pH=6,pH小于6的为酸性溶液,大于6的为碱性溶液,pH=-lgc(H+),强酸和强碱反应的混合溶液呈中性时,氢离子和氢氧根离子的物质的量相等,注意碱性溶液中氢氧根离子浓度的计算方法.
解答 解:100℃的温度下,水的离子积KW=1×10-12,该温度下的中性溶液中pH=6,
A.0.05 mol•L-1的硫酸溶液中,c(H+)=0.05 mol•L-1×2=0.1mol/L,该溶液的pH=1,故A正确;
B.0.001mol/L的氢氧化钠溶液,c(H+)=$\frac{1×1{0}^{-12}}{1×1{0}^{-3}}$mol/L=10-9 mol/L,该溶液的pH=9,故B错误;
C.0.005 mol•L-1的硫酸与0.01 mol•L-1的氢氧化钠溶液等体积时,n(H+)=n(OH-),所以硫酸和氢氧化钠恰好反应,溶液呈中性,反应后溶液的pH为6,故C错误;
D.pH=3的硫酸中,c(H+)=10-3mol/L,pH=11的NaOH溶液中c(OH-)=0.1mol/L,中和pH=3的硫酸溶液50mL,需要pH=11的NaOH溶液0.5mL,故D错误;
故选A.
点评 本题考查pH的简单计算,题目难度不大,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握pH的概念及表达式,试题培养了学生的分析能力及化学计算能力.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙在水中溶解度很小,其溶液的电阻率很大,所以碳酸钙是弱电解质 | |
| B. | 碳酸钙在水中的溶解度很小,但被溶解的碳酸钙全部电离,所以碳酸钙是强电解质 | |
| C. | 氯气和氨气的水溶液导电性都很好,所以它们是强电解质 | |
| D. | 水难电离,纯水几乎不导电,所以水是非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
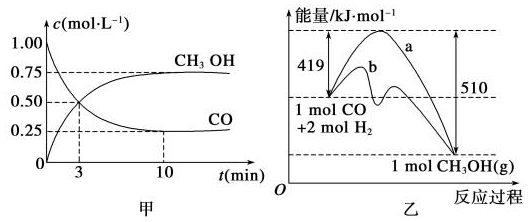
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
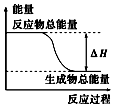
| A. | 铝粉与氧化铁在加热条件下的反应 | |
| B. | 灼热的碳与二氧化碳反应 | |
| C. | Ba(OH)2•8H2O晶体和NH4Cl晶体混合 | |
| D. | 碳与水高温条件下制取水煤气的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
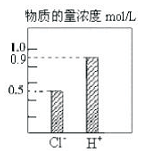 l00mL稀H2S04和稀HC1的混合溶液中,部分离子的浓度关系如图所示,
l00mL稀H2S04和稀HC1的混合溶液中,部分离子的浓度关系如图所示,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在含有大量Al3+的无色溶液中:Cu2+、Na+、Cl-、SO42- | |
| B. | 在含有大量H+的溶液中:Na+、K+、CO32-、NO3- | |
| C. | 在强酸的溶液中:NH4+、Na+、SO42-、Cl- | |
| D. | 在滴加石蕊显蓝色的溶液中:K+、Cu2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
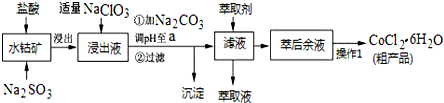
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
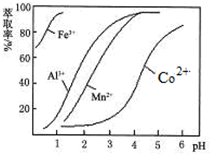
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
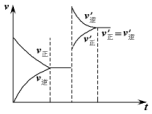 如图表示在密闭容器中反应C(s)+H2O(g)$\stackrel{高温}{?}$CO(g)+H2(g);△H>0,达到平衡后,由于条件的改变而引起正、逆反应速率的变化,以及平衡移动的状况.据图可知,改变的条件是( )
如图表示在密闭容器中反应C(s)+H2O(g)$\stackrel{高温}{?}$CO(g)+H2(g);△H>0,达到平衡后,由于条件的改变而引起正、逆反应速率的变化,以及平衡移动的状况.据图可知,改变的条件是( )| A. | 增加CO浓度 | B. | 升高温度 | C. | 增加水蒸气 | D. | 增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小苏打 | B. | 增白剂 | C. | 蔗糖 | D. | 食盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com