
| A、非金属元素的原子最外层电子数都大于或等于4 |
| B、只有非金属能形成含氧酸或含氧酸盐 |
| C、非金属元素组成的化合物中可能含有离子 |
| D、非金属的最高价含氧酸都具有强氧化性 |


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
| A、c(ClO-)>c(HCO3-)>c(H+) |
| B、c(HCO3-)>c(ClO-)>c(OH-) |
| C、c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3) |
| D、c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,33.6 L氯气与27 g铝充分反应,转移电子数为3NA |
| B、5.6 g铁与足量的稀硫酸反应,失去电子数为0.3NA |
| C、7.8克过氧化钠与足量的水反应,转移的电子总数为0.1 NA |
| D、1 L 1 mol?L-1 Na2CO3溶液中含有NA个CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀释浓硫酸时,应将浓硫酸沿杯壁缓慢倒入盛有水的烧杯中,并用玻璃棒搅拌散热 |
| B、常温下,铝遇浓硫酸、浓硝酸时发生钝化,可以用铝制容器贮存浓硫酸或浓硝酸 |
| C、工业上采用电解熔融MgO的方法制备金属Mg |
| D、往火柴杆上涂抹浓硫酸后出现发黑现象,说明浓H2SO4具有脱水性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、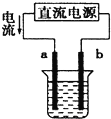 a为阳极,b为阴极 |
B、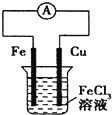 发生的总反应为:Cu+2Fe3+=2Fe2++Cu2+ |
C、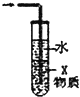 若X为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 |
D、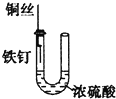 铁钉几乎不发生腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、电解饱和MgCl2溶液:2Cl-+2H2O
| ||||
| B、NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32?+H2O | ||||
| C、硫化亚铁溶于稀盐酸中:FeS+2H+=Fe2++H2S↑ | ||||
| D、Cu粉和稀HNO3 反应:Cu+2NO3-+4H+=Cu2++2NO2↑+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、再通入少量氯气,
| ||
| B、通入少量SO2,溶液漂白性增强 | ||
| C、加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-) | ||
| D、加入少量水,水的电离平衡向正反应方向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com