
| A. | 单位时间内生成a mo1 O2的同时生成2a mol NO2 | |
| B. | 单位时间内生成a mol O2的同时生成2a mol NO | |
| C. | 混合气体的颜色不再改变 | |
| D. | 混合气体的压强不再改变 |
分析 此题列出了判断可逆反应是否达到平衡状态的各种可能情况,应从平衡状态的两个重要特征上判断(1)v(正)=v(逆),(2)混合物中各组成成分的百分含量不变,由此分析解答.
解答 解:A、单位时间内生成a mo1 O2,等效于消耗2a mol NO2同时生成2a mol NO2,反应达平衡状态,故A不选;
B、都反映的正反应,未体现正与逆的关系,故B选;
C、混合气体的颜色不再改变,说明二氧化氮的浓度不变,反应达平衡状态,故C不选;
D、混合气体的压强不再改变,说明各物质的量不变,反应达平衡状态,故D不选;
故选B.
点评 本题考查化学平衡状态的判断,注意分析时要从化学方程式的反应特征判断,平衡状态的本质时正逆反应速率相等.


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 棉花、羊毛、木材和草类的纤维都是天然纤维,人造毛、人造丝是合成纤维 | |
| B. | 哥本哈根会议重点讨论了地球环境问题,其中破坏臭氧层的氟氯代烷是一类多卤代烃,主要含氟和氯的烷烃衍生物,有的还含有溴原子 | |
| C. | 煤的干馏产物有焦炭、煤焦油、焦炉气、粗氨水和粗苯等 | |
| D. | 肥皂和合成洗涤剂的去污原理相似,固态的合成洗涤剂就是洗衣粉,加入蛋白酶可以提高对血迹、奶迹等蛋白质污物的去污能力 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可燃性气体的验纯 | |
| B. | 实验剩余的药品不能放回原试剂瓶 | |
| C. | 滴管不能交叉使用 | |
| D. | 气体实验装置在实验前进行气密性检查 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、SO42-、MnO4- | B. | Ca2+、NH4+、Cl-、NO3- | ||
| C. | Mg2+、K+、HCO3-、Cl- | D. | Na+、K+、SO32-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
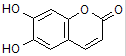
| A. | M的相对分子质量是180 | |
| B. | 1 mol M最多能与2 mol Br2发生反应 | |
| C. | M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4 | |
| D. | 1 mol M与足量NaHCO3反应能生成2 mol CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
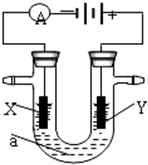 变”)
变”)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Q1>Q3>Q2 | B. | Q3>Q2>2Q1 | C. | Q2>Q3>2Q1 | D. | Q3>2Q1>Q2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 目的 | 分离方法 | 原理 |
| A | 分离溶于水中的碘 | 乙醇萃取 | 碘在乙醇中的溶解度较大 |
| B | 分离氯化钠和碘的固体混合物 | 加热法 | 碘单质易升华 |
| C | 除去KNO3固体中混杂的NaCl | 重结晶 | NaCl在水中的溶解度很大 |
| D | 除去NaOH溶液中的Na2SO4 | 加适量的BaCl2后过滤 | BaSO4难溶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com