
| A、H2SO4 |
| B、HCl |
| C、NaOH |
| D、NaNO3 |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、NO3-、Al3+、Cl- |
| B、Na+、CH3COO-、K+、NO3- |
| C、MnO4-、K+、SO42-、Na+ |
| D、Ca2+、Mg2+、HCO3-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
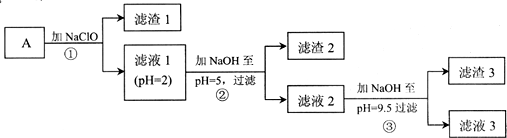
| 物质 | 开始沉淀的pH | 沉淀完全的pH | Kap(25℃) |
| Fe(OH)3 | 2.7 | 3.7 | 4.0×10-38 |
| Fe(OH)2 | 7.6 | 9.6 | 8.0×10-16 |
| Ni(OH)2 | 7.2 | 9.2 | 5.5×10-16 |
| Mg(OH)2 | 9.6 | 11.1 | 1.2×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲、乙两溶液均呈酸性 |
| B、甲、乙两溶液中c(H+)之比为1:2 |
| C、甲、乙两溶液中水的电离程度大小无法比较 |
| D、甲中水的电离程度小于乙中水的电离程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
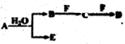 A、B、C、D、E、F为中学化学中的常见物质,且物质A由1-2种短周期元素组成,在一定条件下有如下转化关系,请外完成下列问题:
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1-2种短周期元素组成,在一定条件下有如下转化关系,请外完成下列问题:| 1 |
| 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 亚硝酸钠(NaNO2)易溶于水,微溶于乙醚,是常用的食品发色剂
亚硝酸钠(NaNO2)易溶于水,微溶于乙醚,是常用的食品发色剂查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com