
【题目】化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线如下:
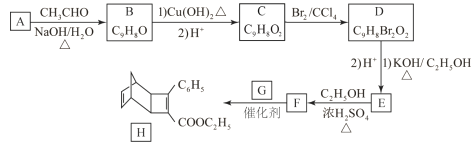
已知:①RCHO+CH3CHO![]() RCH=CHCHO+H2O
RCH=CHCHO+H2O
②![]()
回答下列问题:
(1)A的化学名称为为__________。
(2)由C生成D的反应类型为__________。
(3)E的结构简式为______________________________。
(4)写出用环戊烷和2-丁炔为原料制备化合物 的合成路线 (其他试剂任选)。______ 。
的合成路线 (其他试剂任选)。______ 。
【答案】苯甲醛加成反应![]()

【解析】
由信息①可知A应含有醛基,且含有7个C原子,应为![]() ,则B为
,则B为![]() ,则C为
,则C为![]() ,D为
,D为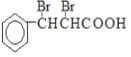 ,E为
,E为![]() ,与乙醇发生酯化反应生成F为
,与乙醇发生酯化反应生成F为![]() ,对比F、H的结构简式可知G为
,对比F、H的结构简式可知G为![]() ,以此解答(1)~(3);(4)环戊烷和2-丁炔为原料制备化合物,环戊烷应先生成环戊烯,然后与2-丁炔发生加成反应生成
,以此解答(1)~(3);(4)环戊烷和2-丁炔为原料制备化合物,环戊烷应先生成环戊烯,然后与2-丁炔发生加成反应生成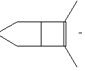 ,最后与溴发生加成可生成
,最后与溴发生加成可生成 ,以此解答该题。
,以此解答该题。
(1)由以上分析可知A为苯甲醛;(2)C为![]() ,发生加成反应生成
,发生加成反应生成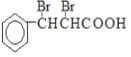 ,E为
,E为![]() ,与乙醇发生酯化反应生成F,也为取代反应;(3)由以上分析可知E为
,与乙醇发生酯化反应生成F,也为取代反应;(3)由以上分析可知E为![]() ;(4)环戊烷和2-丁炔为原料制备化合物
;(4)环戊烷和2-丁炔为原料制备化合物 ,环戊烷应先生成环戊烯,然后与2-丁炔发生加成反应生成
,环戊烷应先生成环戊烯,然后与2-丁炔发生加成反应生成 ,最后与溴发生加成可生成
,最后与溴发生加成可生成 ,在反应的流程为
,在反应的流程为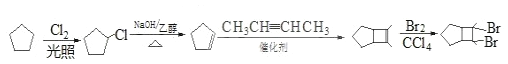 。
。


科目:高中化学 来源: 题型:
【题目】已知反应KClO3 + 6HCl= 3Cl2↑+KCl + 3H2O,下列有关的说法中,正确的是( )
A. HCl 中的Cl 全部被氧化 B. 失电子的氯原子是得电子的氯原子的5倍
C. 反应中有6mol电子发生转移 D. 反应中KClO3 被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常利用以下反应制取少量氮气:NaNO2+NH4Cl![]() NaCl+N2↑+2H2O;关于该反应的下列说法不正确的是( )
NaCl+N2↑+2H2O;关于该反应的下列说法不正确的是( )
A. Na2NO2是氧化剂,NH4Cl是原剂
B. N2既是氧化产物,又是还原产物
C. NH4Cl中氮元素被还原
D. 每生成1molN2转移电子的物质的量为3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法中正确的是( )
A. 已知25 ℃时NH4CN溶液显碱性,则25 ℃时的电离常数K(NH3·H2O)>K(HCN)
B. 室温时, 相同体积、相同pH的盐酸和醋酸溶液中由水电离出的c(H+):盐酸小于醋酸溶液
C. 已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12,向含有Cl-、CrO42-且浓度均为0.010 mol·L-1溶液中逐滴加入0.010 mol·L-1的AgNO3溶液时, CrO42-先产生沉淀
D. 常温下pH=7的CH3COOH和NaOH混合溶液中,c(Na+)>c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物A:
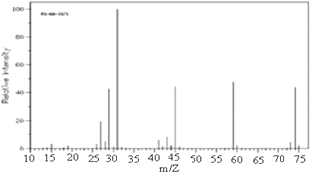
①由C、H、O三种元素组成,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%;
②如图是该有机物的质谱图
③A的红外光谱图上有C-H键、O-H键、C-O键的振动吸收峰.
④A的核磁共振氢谱有两个峰.请回答:
(1)A的实验式(最简式)为_____________,分子式为_____________;
(2)已知A的最简式能否确定A的分子式(填“能”或“不能”)_______,为什么?________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.SO2、CO2、SiO2中的S、C、Si均为sp3杂化
B.H3O+、NH4+、[Cu(NH3)4]2+均含有配位键
C.SO32—、CO32—、SiO32—均为平面三角形
D.石墨、新型高分子导电材料、聚乙烯、金属晶体均含有金属键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】德国重离子研究中心2010年2月19日宣布,由该中心人工合成的第ll2号化学元素从即日起获正式名称“Copemicium”,相应的元素符号为“Cn”。该元素的名称是为了纪念著名天文学家哥白尼而得名。该中心人工合成Cn的过程可表示为:7030Zn+20882Pb→277112Cn+10n。下列叙述中正确的是 ( )
A. 上述合成过程属于化学变化
B. Cn元素位于元素周期表的第七周期,是副族元素
C. Cn元素的相对原子质量为277
D. 277112Cn的原子核内质子数比中子数多53
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由金红石(TiO2)制取单质Ti的反应步骤为:![]()
已知:①C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
③TiO2(s)+2Cl2(g)===TiCl4(s)+O2(g) ΔH=+141 kJ·mol-1
则④TiO2(s)+2Cl2(g)+2C(s)===TiCl4(s)+2CO(g)的ΔH为( )
A. —160 kJ·mol-1 B. +160 kJ·mol-1
C. -80 kJ·mol-1 D. +80 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向NaOH和Na2CO3混合溶液中滴加0.1molL-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图 所示。下列判断正确的是
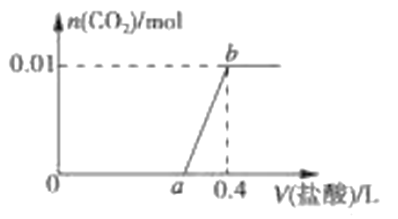
A. 在0a范围内,只发生NaOH和HCl的反应
B. ab段发生反应的离子方程式为:CO32-+2H+=CO2↑+H2O
C. a=0.3
D. 原混合溶液中NaOH与Na2CO3的物质的量之比为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com