
| X | Y | Z | |
| W |
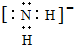
·ÖĪö ÓɶĢÖÜĘŚŌŖĖŲX”¢Y”¢Z”¢WŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆæÉÖŖ£¬X”¢Y”¢Z“¦ÓŚµŚ¶žÖÜĘŚ£¬W“¦ÓŚµŚČżÖÜĘŚ£¬ŌŚĶ¬ÖÜĘŚŌŖĖŲµÄ³£¼ū¼ņµ„Ąė×ÓÖŠ£¬WµÄ¼ņµ„Ąė×Ó°ė¾¶×īŠ”£¬ŌņWĪŖAl£¬æÉĶĘÖŖXĪŖC”¢YĪŖN”¢ZĪŖO£®
£Ø1£©Ö÷×åŌŖĖŲÖÜĘŚŹż=µē×Ó²ćŹż”¢Ö÷×å×åŠņŹż=×īĶā²ćµē×ÓŹż£»
£Ø2£©ŅŗĢ¬NH3ÓėŅŗĢ¬H2OæÉŅŌ·¢ÉśĄąĖĘ·½Ź½µēĄė£¬ŌņŅŗĢ¬NH3ÖŠµēĄėµĆµ½NH4+”¢NH2-£»
£Ø3£©ĀĮ”¢Ńõ»ÆĀĮ¶¼ÓėĒāŃõ»ÆÄʵČĒæ¼īµÄČÜŅŗ·“Ó¦£»
£Ø4£©Al2O3”¢N2”¢CŌŚøßĪĀĻĀ·“Ӧɜ³ÉĮ½ÖÖ»ÆŗĻĪļ£¬ÕāĮ½ÖÖ»ÆŗĻĪļ¾łÓÉĮ½ÖÖŌŖĖŲ×é³É£¬ĒŅŌ×ÓøöŹż±Č¾łĪŖ1£ŗ1£¬·“Ӧɜ³ÉAlNÓėCO£®
½ā“š ½ā£ŗÓɶĢÖÜĘŚŌŖĖŲX”¢Y”¢Z”¢WŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆæÉÖŖ£¬X”¢Y”¢Z“¦ÓŚµŚ¶žÖÜĘŚ£¬W“¦ÓŚµŚČżÖÜĘŚ£¬ŌŚĶ¬ÖÜĘŚŌŖĖŲµÄ³£¼ū¼ņµ„Ąė×ÓÖŠ£¬WµÄ¼ņµ„Ąė×Ó°ė¾¶×īŠ”£¬ŌņWĪŖAl£¬æÉĶĘÖŖXĪŖC”¢YĪŖN”¢ZĪŖO£¬
£Ø1£©XĪŖCŌŖĖŲ£¬Ō×ÓŗĖĶāÓŠ2øöµē×Ó²ć”¢×īĶā²ćµē×ÓŹżĪŖ4£¬“¦ÓŚÖÜĘŚ±ķÖŠµŚ¶žÖܵŚ¢ōA×壬
¹Ź“š°øĪŖ£ŗµŚ¶žÖܵŚ¢ōA×壻
£Ø2£©ŅŗĢ¬NH3ÓėŅŗĢ¬H2OæÉŅŌ·¢ÉśĄąĖĘ·½Ź½µēĄė£¬ŌņŅŗĢ¬NH3ÖŠµēĄėµĆµ½NH4+”¢NH2-£¬NH2-ÖŠNŌ×ÓÓėHŌ×ÓÖ®¼äŠĪ³É1¶Ō¹²ÓƵē×Ó¶Ō£¬Ęäµē×ÓŹ½ĪŖ£ŗ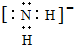 £¬
£¬
¹Ź“š°øĪŖ£ŗ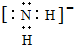 £»
£»
£Ø3£©ĀĮ”¢Ńõ»ÆĀĮ¶¼ÓėĒāŃõ»ÆÄʵČĒæ¼īµÄČÜŅŗ·“Ó¦£¬²»ÄÜÖü“ęĒæ¼īČÜŅŗ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½·Ö±šĪŖAl2O3+2OH-=2AlO2-+H2O”¢2Al+2OH-+2H2O=2AlO2-+3H2”ü£¬
¹Ź“š°øĪŖ£ŗAl2O3+2OH-=2AlO2-+H2O”¢2Al+2OH-+2H2O=2AlO2-+3H2”ü£»
£Ø4£©Al2O3”¢N2”¢CŌŚøßĪĀĻĀ·“Ӧɜ³ÉĮ½ÖÖ»ÆŗĻĪļ£¬ÕāĮ½ÖÖ»ÆŗĻĪļ¾łÓÉĮ½ÖÖŌŖĖŲ×é³É£¬ĒŅŌ×ÓøöŹż±Č¾łĪŖ1£ŗ1£¬·“Ӧɜ³ÉAlNÓėCO£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗAl2O3+N2+3C $\frac{\underline{\;øßĪĀ\;}}{\;}$2AlN+3CO£¬
¹Ź“š°øĪŖ£ŗAl2O3+N2+3C $\frac{\underline{\;øßĪĀ\;}}{\;}$2AlN+3CO£®
µćĘĄ ±¾Ģāæ¼²é½į¹¹ŠŌÖŹ¹ŲĻµÓ¦ÓĆ£¬Éę¼°µē×ÓŹ½”¢Ąė×Ó·“Ó¦µČÖŖŹ¶£¬ĶʶĻÓ¦ŹĒ½āĢā¹Ų¼ü£¬²ąÖŲ¶Ōѧɜ×ŪŗĻÄÜĮ¦Óė»ł“”ÖŖŹ¶µÄÕĘĪÕ£¬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ź³Ę·°ü×°“üÖŠ³£·ÅČėŠ”“ü»¹ŌĢś·Ū£¬ÄæµÄŹĒ·ĄÖ¹Ź³Ę·Ńõ»Æ±äÖŹ | |
| B£® | ĀĮ±ķĆęÓŠŅ»²ćÖĀĆܵÄŃõ»ÆĤ£¬¹ŹĀĮÖĘČŻĘ÷æÉŅŌÓĆĄ“ėēÖĘĻĢ²ĖµČ | |
| C£® | ”°°£²©Ą”±²”¶¾ŌŚ³£ĪĀĻĀ½ĻĪČ¶Ø£¬¶ŌČČÓŠÖŠµČ¶ČµÖæ¹Į¦£¬56”ę²»ÄÜĶźČ«Ćš»ī£¬60”ę30min·½ÄÜĘĘ»µĘäøŠČ¾ŠŌ£¬“Ė¹ż³ĢÖ÷ŅŖ·¢ÉśĮĖµ°°×ÖŹµÄ±äŠŌ | |
| D£® | ĪŖ·ĄÖ¹µē³ŲÖŠµÄÖŲ½šŹōµČĪŪČ¾ĶĮČĄŗĶĖ®Ģ壬Ӧ»ż¼«æŖ·¢·Ļµē³ŲµÄ×ŪŗĻĄūÓĆ¼¼Źõ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ŅŅ“¼ | B£® |  ½šŹōÄĘ | C£® |  ĢģČ»Ęų | D£® |  ŅŅĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
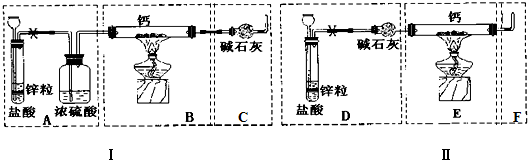
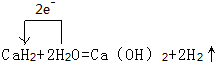 £¬½įŗĻÉĻŹö·“Ó¦£¬ŹµŃé½įŹųŗ󣬼×Ķ¬Ń§Č”ÉŁĮæ²śĪļ£¬Š”ŠÄ¼ÓČėĖ®ÖŠ£¬¹Ū²ģµ½ÓŠĘųÅŻĆ°³ö£¬ČÜŅŗÖŠ¼ÓČė·ÓĢŖŗóĻŌŗģÉ«£¬øĆĶ¬Ń§¾Ż“ĖĶʶĻ£¬ÉĻŹöŹµŃéČ·ÓŠCaH2Éś³É£®ĒėÄć·ÖĪöøĆĶ¬Ń§µÄÅŠ¶ĻŹĒ·ńŗĻĄķ£æ£ØĢī”°ŹĒ”±»ņ”°·ń”±£©£®Čō²»ŗĻĄķ½āŹĶŌŅņ£ØČōÅŠ¶ĻŗĻĄķ£¬“ĖĪŹ²»ÓĆĮ½“š£©·ń£¬½šŹōøĘŗĶĖ®·“Ó¦Ņ²ÓŠĻąĖʵďµŃéĻÖĻó
£¬½įŗĻÉĻŹö·“Ó¦£¬ŹµŃé½įŹųŗ󣬼×Ķ¬Ń§Č”ÉŁĮæ²śĪļ£¬Š”ŠÄ¼ÓČėĖ®ÖŠ£¬¹Ū²ģµ½ÓŠĘųÅŻĆ°³ö£¬ČÜŅŗÖŠ¼ÓČė·ÓĢŖŗóĻŌŗģÉ«£¬øĆĶ¬Ń§¾Ż“ĖĶʶĻ£¬ÉĻŹöŹµŃéČ·ÓŠCaH2Éś³É£®ĒėÄć·ÖĪöøĆĶ¬Ń§µÄÅŠ¶ĻŹĒ·ńŗĻĄķ£æ£ØĢī”°ŹĒ”±»ņ”°·ń”±£©£®Čō²»ŗĻĄķ½āŹĶŌŅņ£ØČōÅŠ¶ĻŗĻĄķ£¬“ĖĪŹ²»ÓĆĮ½“š£©·ń£¬½šŹōøĘŗĶĖ®·“Ó¦Ņ²ÓŠĻąĖʵďµŃéĻÖĻó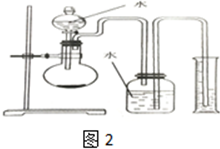
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
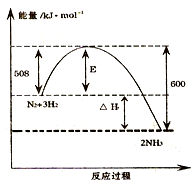 ČēĶ¼±ķŹ¾ĮĖ298KŹ±µŖĘųÓėĒāĘųŗĻ³É°±·“Ó¦¹ż³ĢÖŠµÄÄÜĮæ±ä»Æ£¬¾Ż“ĖĒė»Ų“š£ŗ
ČēĶ¼±ķŹ¾ĮĖ298KŹ±µŖĘųÓėĒāĘųŗĻ³É°±·“Ó¦¹ż³ĢÖŠµÄÄÜĮæ±ä»Æ£¬¾Ż“ĖĒė»Ų“š£ŗ 2NH3£Øg£©”÷H=-92kJ/mol£®
2NH3£Øg£©”÷H=-92kJ/mol£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ³£Ń¹ĻĀCH4ŹĒŅŗĢå | B£® | Ņ»ĀČ¼×Ķé·Ö×ÓŹ½ĪŖCH4Cl | ||
| C£® | CH4ÓėCl2æÉŅŌ·¢Éś¼Ó³É·“Ó¦ | D£® | CH4ĶźČ«Č¼ÉÕÉś³ÉCO2ŗĶH2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
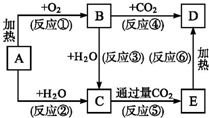 æņĶ¼ÖŠAĪŖŅ»ÖÖ³£¼ūµÄµ„ÖŹ£¬B”¢C”¢D”¢EŹĒŗ¬AŌŖĖŲµÄ³£¼ū»ÆŗĻĪļ£¬ĖüĆĒµÄŃęÉ«·“Ó¦¾łĪŖ»ĘÉ«£®
æņĶ¼ÖŠAĪŖŅ»ÖÖ³£¼ūµÄµ„ÖŹ£¬B”¢C”¢D”¢EŹĒŗ¬AŌŖĖŲµÄ³£¼ū»ÆŗĻĪļ£¬ĖüĆĒµÄŃęÉ«·“Ó¦¾łĪŖ»ĘÉ«£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com