
”¾ĢāÄæ”æ£Ø27·Ö£©
£Ø1£©¼×ĶéŗĶĀČĘų·¢ÉśµÄŅ»ĻµĮŠ·“Ó¦¶¼ŹĒ””””””______·“Ó¦,Š“³öµŚŅ»²½·“Ó¦µÄ»Æѧ·½³ĢŹ½””””””””””____________________________________________”£
£Ø2£©·Ö×ÓÖŠŗ¬ÓŠ34øöĒāŌ×ÓµÄĶéĢžŹĒ””””””______(ĢīĆū³Ę)£¬ŅŅĻ©µÄ½į¹¹¼ņŹ½ĪŖ_____________________£¬ĢĒÄņ²”»¼ÕßÄņŅŗÖŠŗ¬µÄĢĒĄąµÄ·Ö×ÓŹ½ ”£
£Ø3£©ĻÖÓŠĖÄÖÖŹŌ¼Į:A.ŠĀÖʵÄCu(OH)2;B.ÅØĻõĖį;C.AgNO3ČÜŅŗ;D.µāĖ®”£ĪŖĮĖ¼ų±šĻĀĮŠĖÄĘæĪŽÉ«ČÜŅŗ,ĒėÄćŃ”ŌńŗĻŹŹµÄŹŌ¼Į,½«ĘäĢīČėĻąÓ¦µÄĄØŗÅÖŠ”£
¢ŁĘĻĢŃĢĒČÜŅŗ(””””””””)”””” ¢ŚŹ³ŃĪČÜŅŗ(””””””””””)
¢Ūµķ·ŪČÜŅŗ(””””””””””)”””” ¢Ü¼¦µ°ĒåČÜŅŗ(””””””””””)
£Ø4£©½«ĻĀĮŠø÷×齚ŹōÓėĘä¶ŌÓ¦µÄ×ī¼ŃŅ±Į¶·½·ØÓĆĻßĮ¬ĘšĄ“£ŗ
½šŹō×é Ņ±Į¶·½·Ø
Fe”¢Zn”¢CuµČÖŠµČ»īĘĆµÄ½šŹō ĄūÓĆĀĮČČ·“Ó¦ŌĄķÓĆAl»¹Ō
Na”¢Mg”¢AlµČ»īĘĆ½šŹō ŅŌC”¢CO»ņ H2 ×÷»¹Ō¼Į»¹Ō
Hg”¢AgµČ²»»īĘĆ½šŹō µē½ā·Ø
V”¢Cr”¢Mn”¢WµČøßČŪµć½šŹō ČČ·Ö½ā·Ø
”¾“š°ø”æ£Ø1£©Č”“ś CH4£«Cl2![]() CH3Cl£«HCl £Ø2£©Ź®ĮłĶé CH2£½CH2 C6H12O6
CH3Cl£«HCl £Ø2£©Ź®ĮłĶé CH2£½CH2 C6H12O6
£Ø3£©¢ŁA”” ¢ŚC ¢ŪD”” ¢ÜB
 £Ø4£©Fe”¢Zn”¢CuµČÖŠµČ»īĘĆµÄ½šŹō ĄūÓĆĀĮČČ·“Ó¦ŌĄķÓĆAl»¹Ō
£Ø4£©Fe”¢Zn”¢CuµČÖŠµČ»īĘĆµÄ½šŹō ĄūÓĆĀĮČČ·“Ó¦ŌĄķÓĆAl»¹Ō
Na”¢Mg”¢AlµČ»īĘĆ½šŹō ŅŌC”¢CO»ņ H2 ×÷»¹Ō¼Į»¹Ō
Hg”¢AgµČ²»»īĘĆ½šŹō µē½ā·Ø
V”¢Cr”¢Mn”¢WµČøßČŪµć½šŹō ČČ·Ö½ā·Ø
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ£Ø1£©¼×ĶéŗĶĀČĘų·¢ÉśµÄŅ»ĻµĮŠ·“Ó¦¶¼ŹĒČ”“ś·“Ó¦£¬ĘäÖŠµŚŅ»²½·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖCH4£«Cl2![]() CH3Cl£«HCl”£
CH3Cl£«HCl”£
£Ø2£©·Ö×ÓÖŠŗ¬ÓŠ34øöĒāŌ×ÓµÄĶéĢžŹĒ£¬Ōņ2n£«2£½34£¬½āµĆn£½16£¬ĖłŅŌøĆĶéĢžŹĒŹ®ĮłĶ飻ŅŅĻ©µÄ½į¹¹¼ņŹ½ĪŖCH2£½CH2£¬ĢĒÄņ²”»¼ÕßÄņŅŗÖŠŗ¬µÄĢĒĄąŹĒĘĻĢŃĢĒ£¬·Ö×ÓŹ½ĪŖC6H12O6”£
£Ø3£©ĘĻĢŃĢĒÄÜÓėŠĀÖʵÄĒāŃõ»ÆĶŠü×ĒŅŗ·“Ӧɜ³ÉŗģÉ«³Įµķ£¬æÉÓĆÓŚ¼ģŃéĘĻĢŃĢĒ£»Ź³ŃĪĖ®ÄÜÓėĻõĖįŅųČÜŅŗ·“Ó¦²śÉś°×É«³Įµķ£¬æÉÓĆĻõĖįŅųČÜŅŗ¼ģŃ飻µāÓöµķ·ŪĻŌĄ¶É«£¬æÉŅŌÓƵāĖ®¼ģŃéµķ·Ū£»¼¦µ°ĒåÖŠµÄÖ÷ŅŖ³É·ÖŹĒµ°°×ÖŹ£¬æÉŅŌÅØĻõĖį·¢ÉśĻŌÉ«·“Ó¦£»
£Ø4£©Fe”¢Zn”¢CuµČÖŠµČ»īĘĆµÄ½šŹōŅ»°ćÓĆŅŌC”¢CO»ņ H2 ×÷»¹Ō¼Į»¹Ō£»Na”¢Mg”¢AlµČ»īĘĆ½šŹōŅ»°ćÓƵē½ā·ØŅ±Į¶£»Hg”¢AgµČ²»»īĘĆ½šŹōæÉÓĆČČ·Ö½ā·Ø»¹Ō£»V”¢Cr”¢Mn”¢WµČøßČŪµć½šŹōæÉÓĆĀĮČČ·“Ó¦»¹Ō”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŖÖ¤Ć÷ijČÜŅŗÖŠ²»ŗ¬Fe3+¶ųæÉÄÜŗ¬Fe2+£¬½ųŠŠČēĻĀŹµŃé²Ł×÷Ź±µÄ×ī¼ŃĖ³ŠņĪŖ£Ø£©
¢Ł¼ÓČĖÉŁĮæĀČĖ® ¢Ś¼ÓČĖÉŁĮæKMnO4ČÜŅŗ ¢Ū¼ÓČĖÉŁĮæKSCNČÜŅŗ
A£®¢Ł¢Ū B£®¢Ū¢Ś C£®¢Ū¢Ł D£®¢Ś¢Ł
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄ³Ń§Éś×öĶźŹµŃéŗ󣬲ÉÓĆŅŌĻĀ·½·Ø·Ö±šĒåĻ“ĖłÓĆŅĒĘ÷£¬ĘäÖŠĒåĻ“·½·Ø²»ŗĻĄķµÄŹĒ£Ø £©
A. ÓĆ¾Ę¾«ĒåĻ“×ö¹żµāÉż»ŖµÄÉÕ±
B. ÓĆĖ®ĒåĻ“×ö¹żŅų¾µ·“Ó¦µÄŹŌ¹Ü
C. ÓĆÅØŃĪĖįĒåĻ“×ö¹żøßĆĢĖį¼Ų·Ö½āŹµŃéµÄŹŌ¹Ü
D. ÓĆĒāŃõ»ÆÄĘČÜŅŗĒåĻ“Ź¢¹ż±½·ÓµÄŹŌ¹Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøõĢśæóµÄÖ÷ŅŖ³É·ÖæɱķŹ¾ĪŖFeO”¤Cr2O3£¬»¹ŗ¬ÓŠMgO”¢Al2O3”¢Fe2O3µČŌÓÖŹ£¬ŅŌøõĢśæóĪŖŌĮĻÖʱøÖŲøõĖį¼Ų(K2Cr2O7)µÄ¹¤ŅÕČēĻĀ(²æ·Ö²Ł×÷ŗĶĢõ¼žĀŌ)£ŗ
¢ń.½«øõĢśæóŗĶĢ¼ĖįÄĘ»ģŗĻ³ä·Ö±ŗÉÕ”£
¢ņ.±ŗÉÕŗóµÄ¹ĢĢå¼ÓĖ®½žČ”£¬·ÖĄėµĆµ½ČÜŅŗAŗĶ¹ĢĢåA”£
¢ó.ĻņČÜŅŗAÖŠ¼ÓČė“×Ėįµ÷pHŌ¼7”«8£¬·ÖĄėµĆµ½ČÜŅŗBŗĶ¹ĢĢåB”£
¢ō.ŌŁĻņČÜŅŗBÖŠ¼ĢŠų¼Ó“×ĖįĖį»Æ£¬Ź¹ČÜŅŗpHŠ”ÓŚ5”£
¢õ.ĻņÉĻŹöČÜŅŗÖŠ¼ÓČėĀČ»Æ¼Ų£¬µĆµ½ÖŲøõĖį¼Ų¾§Ģ唣
(1)¢ńÖŠ±ŗÉÕ·¢ÉśµÄ·“Ó¦ČēĻĀ£¬ÅäĘ½²¢ĢīŠ“æÕȱ£ŗ
FeOCr2O3 + Na2CO3 + ![]() Na2CrO4 + Fe2O3 + CO2”ü£»
Na2CrO4 + Fe2O3 + CO2”ü£»
¢ŚNa2CO3+Al2O3=2NaAlO2+CO2”ü”£
(2)¹ĢĢåAÖŠÖ÷ŅŖŗ¬ÓŠ (ĢīŠ“»ÆѧŹ½)”£
(3)ŅŃÖŖÖŲøõĖį¼ŲČÜŅŗÖŠ“ęŌŚČēĻĀĘ½ŗā£ŗ2CrO42-£«2H+![]() Cr2O72-£«H2O”£¢ōÖŠµ÷½ŚČÜŅŗpH£¼5Ź±£¬ĘäÄæµÄŹĒ ”£
Cr2O72-£«H2O”£¢ōÖŠµ÷½ŚČÜŅŗpH£¼5Ź±£¬ĘäÄæµÄŹĒ ”£
(4)¢õÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ£ŗNa2Cr2O7+2KCl=K2Cr2O7”ż+2NaCl£¬ŅŃÖŖĻĀ±ķŹż¾Ż
ĪļÖŹ | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
Čܽā¶Č (g/100gĖ®) | 0”ę | 28[Ą“ | 35.7 | 4.7 | 163 |
40”ę | 40.1 | 36.4 | 26.3 | 215 | |
80”ę | 51.3 | 38 | 73 | 376 | |
¢ŁøĆ·“Ó¦ÄÜ·¢ÉśµÄĄķÓÉŹĒ ”£
¢Ś»ńµĆK2Cr2O7¾§ĢåµÄ²Ł×÷ÓŠ¶ą²½×é³É£¬ŅĄ“ĪŹĒ£ŗ¼ÓČėKCl¹ĢĢ唢 ”¢ ”¢¹żĀĖ”¢Ļ“µÓ”¢øÉŌļµĆµ½¾§Ģ唣
(5)¢óÖŠ¹ĢĢåBÖŠÖ÷ŅŖŗ¬ĒāŃõ»ÆĀĮ£¬»¹ŗ¬ÉŁĮæĆ¾”¢ĢśµÄÄŃČÜ»ÆŗĻĪļ¼°æÉČÜŠŌŌÓÖŹ£¬¾«Č··ÖĪö¹ĢĢåBÖŠĒāŃõ»ÆĀĮŗ¬ĮæµÄ·½·ØŹĒ£ŗ³ĘČ”n gѳʷ£¬¼ÓČė¹żĮæ________(ĢīŠ“ŹŌ¼ĮĆū³Ę)”¢Čܽā”¢¹żĀĖ”¢ŌŁĶØČė¹żĮæµÄCO2”¢”×ĘÉÕ”¢ĄäČ“”¢³ĘĮ棬µĆøÉŌļ¹ĢĢåm g”£¼ĘĖćѳʷ֊ĒāŃõ»ÆĀĮµÄÖŹĮæ·ÖŹżĪŖ______ (ÓĆŗ¬m”¢nµÄ“śŹżŹ½±ķŹ¾)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ĖłŹ¾£¬”÷H1=©393.5kJmol©1£¬”÷H2=©395.4kJmol©1£¬ĻĀĮŠĖµ·Ø»ņ±ķŹ¾Ź½ÕżČ·µÄŹĒ£Ø £©
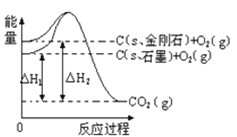
A£®C£Øs”¢ŹÆÄ«£©ØTC£Øs”¢½šøÕŹÆ£©”÷H=©1.9 kJmol©1
B£®ŹÆÄ«µÄĪČ¶ØŠŌĒæÓŚ½šøÕŹÆ
C£®ŹÆÄ«ŗĶ½šøÕŹÆµÄ×Ŗ»ÆŹĒĪļĄķ±ä»Æ
D£®1 molŹÆÄ«µÄ×ܼüÄܱČ1 mol½šøÕŹÆµÄ×ܼüÄÜŠ”1.9 kJ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹōÓŚ»Æѧ±ä»ÆµÄŹĒ£Ø £©
A£®Ļņ±„ŗĶµÄĮņĖįļ§ČÜŅŗÖŠµĪ¼Óµ°ĒåČÜŅŗ
B£®ČÕ±¾ŗĖµēÕ¾¹¤×÷ČĖŌ±øųŗĖµē»ś×é×¢Ė®½µĪĀ
C£®Į¶ÓĶ³§ÕōĮóŌÓĶ»ńµĆĘūÓĶ”¢ĆŗÓĶµČ²śĘ·
D£®Ā¶ÖĆÓŚæÕĘųÖŠµÄĆ¾“ų±ķĆęÖš½„±äŗŚ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æKClO3ŗĶÅØŃĪĖįŌŚŅ»¶ØĪĀ¶ČĻĀ·“Ó¦»įÉś³É»ĘĀĢÉ«µÄŅ×±¬Īļ¶žŃõ»ÆĀČ”£Ęä±ä»ÆæɱķŹöĪŖ£ŗ 2KClO3 £«4HCl(ÅØ)=2KCl£«2ClO2”ü£«Cl2”ü£«2H2O”£
£Ø1£©Ēė·ÖĪöøĆ·“Ó¦ÖŠµē×Ó×ŖŅʵÄĒéæö£ŗ(µ„ĻßĒŷرķŹ¾)________________________”£
£Ø2£©Ńõ»Æ¼ĮÓė»¹Ō¼ĮµÄĪļÖŹµÄĮæÖ®±ČŹĒ ___________________
£Ø3£©Čō²śÉś±źæöĻĀ22.4 L Cl2£¬Ōņ×ŖŅʵĵē×ÓµÄĪļÖŹµÄĮæĪŖ________mol”£
£Ø4£©ŹµŃéŹŅ±øÓƵÄÅØŃĪĖįÖŹĮæ·ÖŹżĪŖ36.5%£¬ĆܶČĪŖ1.19 g”¤cm-3£¬ĪŖŹ¹ÓĆ·½±ć,Ēė¼ĘĖć³öøĆÅØŃĪĖįÖŠHClµÄĪļÖŹµÄĮæÅØ¶Č mol”¤L-1”£
£Ø5£©ClO2¶ŌĪŪĖ®ÖŠFe2£«”¢Mn2£«”¢S2-ŗĶCN- µČÓŠĆ÷ĻŌµÄČ„³żŠ§¹ū”£Ä³¹¤³§ĪŪĖ®ÖŠŗ¬CN- a mg/L£¬ĻÖÓĆClO2½«CN - Ńõ»Æ£¬Ö»Éś³ÉĮ½ÖÖĘųĢ壬ĘäĄė×Ó·“Ó¦·½³ĢŹ½ĪŖĪŖ £¬“¦Ąķ100 m3ÕāÖÖĪŪĖ®£¬ÖĮÉŁŠčŅŖClO2 _______mol”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĄė×Ó·½³ĢŹ½ÖŠ£¬ÕżČ·µÄŹĒ£Ø £©
A£®ÄĘÓėĖ®·“Ó¦£ŗNa+H2O=Na++OH©+H2”ü
B£®ĮņĖįÓėĒāŃõ»Æ±µČÜŅŗ·“Ó¦£ŗH++OH©=H2O
C£®ĢśÓėĮņĖįĢś·“Ó¦£ŗFe+Fe3+=2Fe2+
D£®ĀČ»ÆÄĘČÜŅŗÓėĻõĖįŅųČÜŅŗ·“Ó¦£ŗAg++Cl©=AgCl”ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÖŠ¹śÕžø®³ŠÅµ,µ½2020Äź,µ„Ī»GDP¶žŃõ»ÆĢ¼ÅŷűČ2005ÄźĻĀ½µ40%”«50%”£
£Ø1£©ÓŠŠ§¼õĢ¼µÄŹÖ¶ĪÖ®Ņ»ŹĒ½ŚÄÜ,ĻĀĮŠÖĘĒā·½·Ø×ī½ŚÄܵďĒ ”£
A.µē½āĖ®ÖĘĒā:2H2O![]() 2H2”ü+O2”ü
2H2ӟ+O2ӟ
B.øßĪĀŹ¹Ė®·Ö½āÖĘĒā:2H2O![]() 2H2”ü+O2”ü
2H2ӟ+O2ӟ
C.Ģ«Ńō¹ā“߻ƷֽāĖ®ÖĘĒā:2H2O![]() 2H2”ü+O2”ü
2H2ӟ+O2ӟ
D.ĢģČ»ĘųÖĘĒā:CH4+H2O![]() CO+3H2
CO+3H2
£Ø2£©CO2æÉ×Ŗ»Æ³ÉÓŠ»śĪļŹµĻÖĢ¼Ń»·”£ŌŚĢå»żĪŖ1 L µÄĆܱÕČŻĘ÷ÖŠ,³äČė1 mol CO2ŗĶ3 mol H2,Ņ»¶ØĢõ¼žĻĀ·“Ó¦:CO2£Øg£©+3H2£Øg£©![]() CH3OH£Øg£©+H2O£Øg£© ¦¤H=-49.0 kJ/mol,²āµĆCO2ŗĶCH3OH£Øg£©µÄÅضČĖꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾”£
CH3OH£Øg£©+H2O£Øg£© ¦¤H=-49.0 kJ/mol,²āµĆCO2ŗĶCH3OH£Øg£©µÄÅضČĖꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾”£
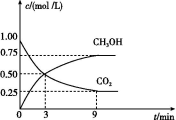
“Ó3 minµ½9 min,v£ØH2£©= mol/£ØL”¤min£©”£
¢ŚÄÜĖµĆ÷ÉĻŹö·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄŹĒ £ØĢī±ąŗÅ£©”£
A.·“Ó¦ÖŠCO2ÓėCH3OHµÄĪļÖŹµÄĮæÅضČÖ®±ČĪŖ1”Ć1£Ø¼“Ķ¼ÖŠ½»²ęµć£©
B.»ģŗĻĘųĢåµÄĆÜ¶Č²»Ėꏱ¼äµÄ±ä»Æ¶ų±ä»Æ
C.µ„Ī»Ź±¼äÄŚĻūŗÄ3 mol H2,Ķ¬Ź±Éś³É1 mol H2O
D.CO2µÄĢå»ż·ÖŹżŌŚ»ģŗĻĘųĢåÖŠ±£³Ö²»±ä
£Ø3£©¹¤ŅµÉĻ,CH3OHŅ²æÉÓÉCOŗĶH2ŗĻ³É”£²Īæ¼ŗĻ³É·“Ó¦CO£Øg£©+2H2£Øg£©![]() CH3OH£Øg£©µÄĘ½ŗā³£Źż:
CH3OH£Øg£©µÄĘ½ŗā³£Źż:
ĪĀ¶Č/”ę | 0 | 100 | 200 | 300 | 400 |
Ę½ŗā³£Źż | 667 | 13 | 1.9”Į1 | 2.4”Į1 | 1”Į1 |
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ ”£
A.øĆ·“Ó¦Õż·“Ó¦ŹĒ·ÅČČ·“Ó¦
B.øĆ·“Ó¦ŌŚÉżøßĪĀ¶ČŹ±,CH3OH£Øg£©µÄĢå»ż·ÖŹż¼õŠ”,ĖµĆ÷vÕż£ØCH3OH£©¼õŠ”,vÄę£ØCH3OH£©Ōö“ó
C.ŌŚT ”ꏱ,1 LĆܱÕČŻĘ÷ÖŠ,Ķ¶Čė0.1 mol COŗĶ0.2 mol H2,“ļµ½Ę½ŗāŹ±,CO×Ŗ»ÆĀŹĪŖ50%,Ōņ“ĖŹ±µÄĘ½ŗā³£ŹżĪŖ100
D.¹¤ŅµÉĻ²ÉÓĆÉŌøßµÄŃ¹Ēæ£Ø5 Mpa£©ŗĶ250 ”ę,ŹĒŅņĪŖ“ĖĢõ¼žĻĀ,ŌĮĻĘų×Ŗ»ÆĀŹ×īøß
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com