
A��B��C����ѧ��ѧ�������������ʣ�����֮����ת����ϵ���£����ַ�Ӧ������������ȥ����
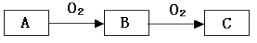
��1����A��һ�ֻ�ɫ���ʹ��壬��B��C�Ļ�ѧ����ʽΪ ��
��2����A��һ�ֻ��ý�����C�ǵ���ɫ���壬��C������Ϊ �����û�ѧ����ʽ��ʾ�������������̼����ķ�Ӧ ����C����¶���ڿ����У���������D��D�Ļ�ѧʽΪ ������D��NaHCO3�Ĺ�������10g���������������ٸı䣬ʣ���������Ϊ9.38 g��D����������Ϊ ��
��3����C�Ǻ���ɫ���壬A������һ����ʹʪ��ĺ�ɫʯ����ֽ���������塣��ͼ��ʵ������ȡA�����װ�ã�������ѧ֪ʶ���ش��������⣺

���ռ�A�ķ����� ����֤A�Ƿ��Ѿ��ռ����ķ����� ����дһ�֣���
��д��ʵ������ȡA�Ļ�ѧ����ʽ ��
������5��35g�Ȼ�鱗μӷ�Ӧ���������A�����ڱ�״���µ����Ϊ L��
����д��C��ˮ��Ӧ�Ļ�ѧ����ʽ ����Ӧ�ɵõ���X��X�� ��
���ʣ�����ǿ������������������ͼ������X��Ũ��Һ��Cu��Ӧ��д����ƿ�з�����Ӧ�����ӷ���ʽ ��ʵ����Ϻ��Թ����ռ������������Ҫ�ɷ�Ϊ ��д��ѧʽ��
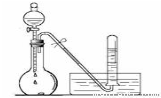
��1��2SO2��O2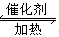 2SO3
2SO3
��2���������� 2Na2O2��2CO2��2 Na2CO3��O2 Na2CO3 83.2%
��3���������ſ����� ��ʪ��ĺ�ɫʯ����ֽ�����Թܿڴ�������ֽ��������֤���������ռ�����
������պ��Ũ����IJ����������Թܿڴ����������������̣���֤���������ռ�����
��Ca(OH)2��2NH4Cl CaCl2��2NH3����2H2O ��2.24
CaCl2��2NH3����2H2O ��2.24
��3NO2��H2O��2 HNO3��NO ǿ Cu��4H����2 NO3-��Cu2����2 NO2����2H2O NO
��������
�����������1����A��һ�ֻ�ɫ���ʹ��壬��A��S���ʣ�����B�Ƕ�������C������������B��C�Ļ�ѧ����ʽΪ2SO2+O2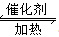 2SO3����2����A��һ�ֻ��ý�����C�ǵ���ɫ���壬��A���ƣ�B�������ƣ�C�ǹ������ƣ��������������տ����е�ˮ����2Na2O2+2H2O=4NaOH+O2�����õ�NaOH��������CO2 ��������ӦΪ��CO2��2NaOH=Na2CO3��H2O;��Һ��ˮ���������γ�Na2CO3��10H2O������绯�õ�Na2CO3������ʱ������Ӧ��2NaHCO3
2SO3����2����A��һ�ֻ��ý�����C�ǵ���ɫ���壬��A���ƣ�B�������ƣ�C�ǹ������ƣ��������������տ����е�ˮ����2Na2O2+2H2O=4NaOH+O2�����õ�NaOH��������CO2 ��������ӦΪ��CO2��2NaOH=Na2CO3��H2O;��Һ��ˮ���������γ�Na2CO3��10H2O������绯�õ�Na2CO3������ʱ������Ӧ��2NaHCO3 Na2CO3��CO2����H2O.n(H2CO3)= 10g-9.38g=0.62g��62g/mol=0.01mol.����n(NaHCO3)=0.02mol��m (NaHCO3)=0.02mol��84g/mol=1.68g
Na2CO3��CO2����H2O.n(H2CO3)= 10g-9.38g=0.62g��62g/mol=0.01mol.����n(NaHCO3)=0.02mol��m (NaHCO3)=0.02mol��84g/mol=1.68g
m(Na2CO3)=10g-1.68g=8.32g�����Na2CO3����������Ϊ(8.32g ��10g )��100%=83.2%��
��3����AΪ��ʹʪ��ĺ�ɫʯ����ֽ���������壬��AӦ���ǰ�����BΪNO��C�Ǻ���ɫ���壬ӦΪNO2����AΪ��������������ˮ�����Բ�������ˮ���ռ������ڰ������ܶȱȿ���С�����������ſ������ռ������鰱���Ƿ��ռ������ɽ�ʪ��ĺ�ɫʯ����ֽ�����Թܿڴ�������ֽ��������֤���������ռ�����������ɫ�ķ�̪��ֽ�����Թܿڴ�������ֽ��죬��֤���������ռ�����Ҳ������պ��Ũ����IJ����������Թܿڴ����������������̣���֤���������ռ�������ʵ�������������ƺ��Ȼ���ڼ��������·�Ӧ����������Ӧ�ķ���ʽΪCa(OH)2��2NH4Cl CaCl2��2NH3����2H2O.��n��NH4Cl��=
CaCl2��2NH3����2H2O.��n��NH4Cl��=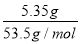 =0.1mol����n��NH3��=0.1mol��V��NH3��=0.1mol ��22.4L/mol=2.24L��
=0.1mol����n��NH3��=0.1mol��V��NH3��=0.1mol ��22.4L/mol=2.24L��
��CΪNO2����ˮ��Ӧ���������NO����Ӧ�ķ���ʽΪ3NO2+H2O=2HNO3+NO��HNO3��ǿ����ʣ�����ǿ�����ԣ�����ͭ��Ӧ����Ӧ�����ӷ���ʽΪCu+4H++2NO3-=Cu2++2NO2��+2H2O��ʵ����Ϻ��Թ����ռ������������Ҫ�ɷ�ΪNO��
���㣺���ʵ��ƶ�����Ԫ�صĵ��ʼ���������ת��������������ʺ����ļ��㡢������ʵ������ȡ���ռ������顢��������ѧ����ʽ�����ӷ���ʽ����д��֪ʶ��


 ����ѧУ�ֲ����ܲ�ϵ�д�
����ѧУ�ֲ����ܲ�ϵ�д� �ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
�ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�����ʡ��һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������ͨ�����з�ɢϵʱ���ܹ۲쵽�����ЧӦ����( )��
A��������Һ B������ C���Ȼ�����Һ D��Fe(OH)3 ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ʵ���Ҽ���KClO3��MnO2�Ļ�������������ʣ��������л���MnO2�IJ���˳����ȷ����( )
A���ܽ⡢���ˡ�������ϴ�� B���ܽ⡢������ϴ�ӡ�����
C���ܽ⡢���ˡ�ϴ�ӡ����� D���ܽ⡢ϴ�ӡ����ˡ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ij���塢����dz��ɫ��Һ�У����ܺ������а������ӣ�H����NH4+��Fe3����Ba2����Al3����SO42-��CO32-��I�����ڼ��鷽�����ʱ������������Һ�����ɺ�����(������OH��)�� �� ��
A��4�� B��5�� C��6�� D��7��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и������ʣ�ǰ�����ڵ���ʣ��������ڷǵ���ʵ��ǣ� ��
A��NaCl���塢BaSO4 B��ͭ����������
C��Һ̬�Ĵ��ᡢ�ƾ� D�����ڵ�KNO3��������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�˲���Э�����һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���������У�������Ũ�������������������Ƹ������
A��CO2 B��N2 C��SO2 D��NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�˲���Э�����һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���в�������ȷ����
A������������ʹNaCl����Һ������ʱ������������NaCl ��Һȫ����������
B����������ƽ�ϳ���NaOHʱ��Ӧ��NaOH�������С�ձ��г���
C����25 mL��Ͳ��ȡ4��0 mol/L������5��62 mL
D����������ƽȷ��ȡ5��85 g NaCl����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�캣��ʡ�����и�һ��ѧ�ڶο���ѧ�Ծ��������棩 ���ͣ�ѡ����
���ӷ�Ӧ�����ֽⷴӦ���û���Ӧ��������ԭ��Ӧ֮����ü��Ϲ�ϵ��ʾ,��ȷ���ǣ� ��
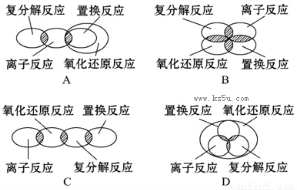
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��һ֧ʢ��a mL NO ��b mL NO2������Թܵ�����ˮ���У�Ȼ��ͨ��a mL O2����ش�����С�⣺
��1����a=b�����ַ�Ӧ���Թ����������Ϊ_________mL��
��2����a��b�����ַ�Ӧ���Թ����������Ϊ_________mL��
��3����a��b�����ַ�Ӧ���Թ����������Ϊ_________mL��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com