
【题目】绿原酸的结构简式如图,下列有关绿原酸的说法错误的是( )
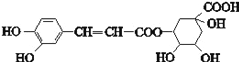
A. 分子式为C16H18O9 B. 能与NaHCO3反应
C. 能发生取代反应、氧化反应和消去反应 D. 1 mol绿原酸最多与6 mol Br2反应
科目:高中化学 来源: 题型:
【题目】拟用如图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。下列可以得到干燥纯净的气体的选项是( )

选项 | 气体 | a | b | c | d |
A | CO2 | 盐酸 | CaCO3 | 饱和Na2CO3溶液 | 浓硫酸 |
B | NH3 | 饱和NH4Cl溶液 | 消石灰 | H2O | 固体NaOH |
C | Cl2 | 浓盐酸 | MnO2 | 饱和NaCl溶液 | 浓硫酸 |
D | NO2 | 浓硝酸 | 铜屑 | H2O | 固体NaOH |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是
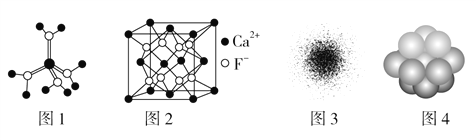
A. 水合铜离子的模型如图1所示,1个水合铜离子中有4个配位键
B. CaF2晶体的晶胞如图2所示,每个CaF2晶胞平均占有4个Ca2+
C. H原子的电子云图如图3所示,H原子核外大多数电子在原子核附近运动
D. 金属铜中Cu原子堆积模型如图4为最密堆积每个Cu原子的配位数均为12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴是人体必需的微量元素,含钴化合物作为颜料,具有悠久的历史,在机械制造、磁性材料等领域也具有广泛的应用,请回答下列问题:
(1)Co基态原子的电子排布式为_____。
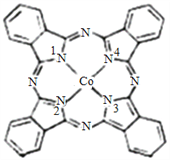
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学中的光敏剂、催化剂等方面得到广泛的应用,其结构如图所示,中心离子为钴离子。
①酞菁钴中三种非金属原子的电负性有大到小的顺序为_________ (用相应的元素符号作答);碳原子的杂化轨道类型为__________;
②与钴离子通过配位键结合的氮原子的编号是_____________。
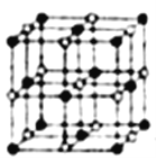
(3)Co的一种氧化物的晶胞如图所示,在该晶体中与一个钴原子等距离且最近的氧原子有______个;已知在该钴的氧化物晶体中钴原子的半径为apm,氧原子的半径为bpm,它们在晶体中是紧密接触的,则在该钴的氧化物晶体中原子的空间利用率为____(用含a、b的式子表示)。
(4)筑波材料科学国家实验室一个科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如下图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图中,不能描述CoO2的化学组成的是_______。
 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的NaHCO3和Na2O2的混合物置于一密闭容器中充分加热,反应中转移的电子数为1mol,下列说法一定正确的是( )
A. 混合物中NaHCO3和Na2O2物质的量一定相等
B. 容器中肯定有0.5molO2
C. 反应后,容器中的固体只有Na2CO3
D. 反应后,容器中一定没有H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学兴趣小组设定以下实验方案,测定某已变质为碳酸钠的小苏打样品中NaHCO3的质量分数。
方案一:称取一定质量样品,置于坩埚中加热至恒重,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为:__________________;
(2)实验中需加热至恒重的目的是:___________________;
方案二:称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤,干燥沉淀,称量固体质量,计算。
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为_____________;
(2)实验中判断沉淀是否完全的方法是_______________________。
方案三:按如图装置进行实验:
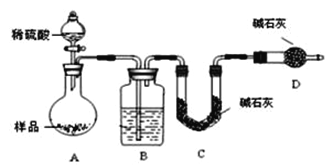
(1)B装置内所盛试剂是_________;D装置的作用是_______;分液漏斗中_______(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.9g样品,实验后测得C装置增重8.8g,则样品中NaHCO3的质量分数为____。
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷是:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蒸馏是实验室制备蒸馏水的常用方法
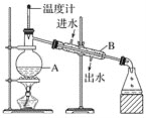
(1)如图是实验室制取蒸馏水的常用装置,图中明显的一个错误是____________________。
(2)仪器A的名称是______________,仪器B的名称是______________。
(3)实验时A中除加入少量自来水外,还需加入几粒____________,其作用是防止液体暴沸。
(4)从锥形瓶取少量收集到的液体于试管中,然后滴入____________和____________(填试剂的化学式),检验是否存在氯离子。
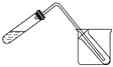
(5)如图装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与上图完全相同。该装置中使用的玻璃导管较长,其作用是______________;烧杯中最好盛有的物质是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:
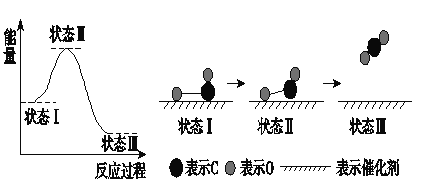
下列说法中正确的是( )
A. CO和O生成了具有共价键的CO2 B. 在该过程中,CO断键形成C和O
C. 状态Ⅰ→状态Ⅲ表示CO与O2反应的过程 D. CO和O生成CO2是吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com