
分析 (1)①该燃料电池中,甲烷和氧气反应生成二氧化碳和水;
②燃料电池中,通入燃料的电极是负极,通入氧化剂的电极是正极,碱性条件下,正极上氧气得电子和水反应生成氢氧根离子;
③根据电池反应式知,随着反应的进行,溶液中KOH参加反应导致浓度降低;
④燃料电池中大部分化学能转化为电能,燃料燃烧时,很多化学能转化为热能、光能等;
(2)①甲醇燃料碱性电池中,甲醇和碱反应生成碳酸根离子和水;
②负极上甲醇失电子发生氧化反应,根据电池反应式中氢氧根离子浓度变化判断pH变化.
解答 解:(1)①该燃料电池中,甲烷和氧气反应生成二氧化碳和水,反应方程式为CH4+2O2=CO2+2H2O,故答案为:CH4+2O2=CO2+2H2O;
②CH4+10OH--8e-═CO32-+7H2O中C元素化合价由-4价变为+4价,所以甲烷失电子发生氧化反应,其所在电极为负极,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为2O2+4H2O+8e-═8OH-,故答案为:负极;2O2+4H2O+8e-═8OH-;
③该燃料电池电池反应式为CH4+10OH--8e-═CO32-+7H2O,氢氧根离子参加反应,所以反应过程中氢氧根离子浓度减小,溶液的pH减小,故答案为:减小.
④燃料电池中大部分化学能转化为电能,燃料燃烧时,很多化学能转化为热能、光能等,所以燃料燃烧能量利用率较低,故答案为:大于;
(2)①甲醇燃料碱性电池中,甲醇和碱反应生成碳酸根离子和水,离子反应方程式为2CH3OH+3O2+4OH-=2CO32-+6H2O,
故答案为:2CH3OH+3O2+4OH-=2CO32-+6H2O;
②负极上甲醇失电子发生氧化反应,根据电池反应式知,氢氧根离子参加反应导致溶液中氢氧根离子浓度降低,所以溶液的pH下降,故答案为:负;降低.
点评 本题考查化学电源新型电池,为高频考点,所有的燃料电池中负极通入燃料、正极通入氧化剂,但电解质有酸性溶液、碱性溶液、熔融盐或熔融氧化物类型,难点是电极反应式的书写.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
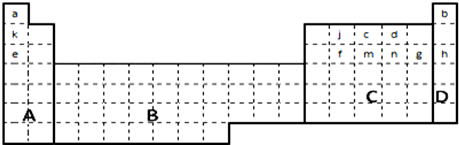
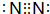 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应产物的总焓与反应物的总焓之差,称为反应焓变 | |
| B. | 反应产物的总焓小于反应物的总焓,该反应为吸热反应 | |
| C. | 同一反应在不同温度下进行,其焓变是不同的 | |
| D. | 已知2NO2(g)═N2O4(g)△H1,N2O4(g)═2NO2(g)△H2,则△H1=-△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Ca(OH)2溶液中加入过量的NaHCO3溶液:Ca2++2OH-+2HCO3-═CaCO3↓+CO32-+2H2O | |
| B. | 硫酸氢钠与氢氧化钡两种溶液反应后pH恰好为7:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| C. | NaHCO3溶液与稀H2SO4反应:CO32-+2H+═CO2↑+2H2O | |
| D. | 铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 构成原电池正极和负极的材料必须是两种金属 | |
| B. | 当由铜、锌电极与硫酸铜溶液组成原电池时,铜是负极 | |
| C. | 负极反应为:2H++2e-═H2↑ | |
| D. | 该装置能将化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体硅是将太阳能转化为电能的常用材料 | |
| B. | 用加热的方法杀死H7N9禽流感病毒是采用了蛋白质变性原理 | |
| C. | “克隆羊”的关键技术之一是找到一些激活普通细胞的酶,并将它浸泡在酒精中保存 | |
| D. | 钠钾合金在常温下呈液态,可用于快中子反应堆作热交换剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,20 g D2O和足量的金属钠反应产生气体的分子数为0.5NA | |
| B. | 1 mol Na2O2与足量的水反应,转移的电子数为2NA | |
| C. | NA 个SO3分子在标准状况下的体积为22.4 L | |
| D. | 25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向10ml 0.1mol•L-1NH4HSO4溶液中滴加10ml 0.1mol•L-1NaOH溶液:2c(SO42-)═c(NH4+)+c(NH3•H2O) | |
| B. | 等体积等浓度NaHCO3溶液和Na2CO3溶液混合:$\frac{C(HC{O}_{3}^{-})}{C({H}_{2}C{O}_{3})}$<$\frac{C(C{O}_{3}^{2-})}{C(HC{O}_{3}^{-})}$ | |
| C. | 物质的量浓度均为0.1mol•L-1Na2S溶液、NaHS溶液等体积混合所得溶液中:2c(OH--)-2c(H+)═3 c(H2S)+c(HS--)-c(S2--) | |
| D. | 将足量的AgCl分别放入:①5 ml水 ②10 ml 0.2mol•L-1MgCl2溶液③20ml0.3mol•L-1盐酸中溶解至饱和,c(Ag+):①>②>③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com