
关于0.1 mol·L-1Na2CO3溶液的叙述中错误的是 ( )
A.0.5 L该溶液中钠离子的物质的量浓度为0.2 mol·L-1
B.1 L该溶液中含有Na2CO3的质量为10.6 g
C.从1 L该溶液中取出100 mL,则取出溶液中Na2CO3的物质的量浓度为
0.01 mol·L-1
D.取该溶液10 mL,加水稀释至100 mL后,Na2CO3的物质的量浓度为0.01 mol·L-1
科目:高中化学 来源: 题型:
太阳能的开发和利用是21世纪一个重要课题。利用储能介质储存太阳能的原理是:白天在太阳照射下某种盐熔化,吸收热量,晚间熔盐固化释放出相应的能量,已知下表数据:
| 盐 | 熔点(℃) | 熔化吸热(kJ·mol-1) | 参考价格(元·t-1) |
| CaCl2·6H2O | 29.9 | 37.3 | 780~850 |
| Na2SO4·10H2O | 32.4 | 77.0 | 800~900 |
| Na2HPO4·12H2O | 35.1 | 100.1 | 1 600~2 000 |
| Na2S2O3·5H2O | 45.0 | 49.7 | 1 400~1 800 |
其中最适宜选用作为储能介质的是( )
A.CaCl2·6H2O B.Na2SO4·10H2O
C.Na2HPO4·12H2O D.Na2S2O3·5H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列物质中:①CO2 ②NaCl ③MgBr2 ④I2 ⑤NH4Cl ⑥Ca(OH)2 ⑦N2 ⑧H2S ⑨NH3
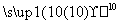 K2O2
K2O2
(1)只有非极性键的是_________________________________;
(2)只有极性键的是___________________________________;
(3)只有离子键的是___________________________________;
(4)有离子键,也有非极性键的是_______________________;
(5)既有离子键,又有极性键的是_______________________;
(6)属于离子化合物的是_______________________________;
(7)属于共价化合物的是_______________________________;
(8)含有配位键的物质是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是 ( )
A.当两种原子的电负性相差很大时,相互之间通常形成离子键
B.不含金属元素的化合物不一定是共价化合物
C.HCl分子中的共价键是由氢原子的1s轨道和氯原子的3s轨道重叠形成的
D.四氯化碳分子中含四个共价单键,为正四面体
查看答案和解析>>
科目:高中化学 来源: 题型:
右图是周期表中短周期的一部分。已知A、B
两元素原子的最外层电子数之和等于E元素原子的最外层电子数。下列有关说法正确
的是
A.元素B和E、B和D形成的化合物在固态时都属于分子晶体
B.工业上可用A、D形成的化合物制取A的单质;B的单质在信息业有广泛用途
C.与E同族的元素中,若简单阴离子的还原性越强,则该元素的最高价氧化物对应水化物的酸性也越
强
D.元素B的最简单氢化物分子的空间构型为正四面体,元素C的最简单氢化物的沸点比E的气态氢
化物的沸点高
查看答案和解析>>
科目:高中化学 来源: 题型:
在200 mL某硫酸盐溶液中,含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子。则该硫酸盐的物质的量浓度为 ( )
A.1 mol·L-1 B.2.5 mol·L-1
C.5 mol·L-1 D.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于原子结构、元素性质的说法正确的是( )
A.非金属元素组成的化合物中只含共价键
B.ⅠA族金属元素是同周期中金属性最强的元素
C.同种元素的原子均有相同的质子数和中子数
D.ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强
查看答案和解析>>
科目:高中化学 来源: 题型:
利用反应2NO(g)+2CO(g)2CO2(g)+N2(g) ΔH=-746.8 kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是( )
A.降低温度
B.增大压强同时加催化剂
C.升高温度同时充入N2
D.及时将CO2和N2从反应体系中移走
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验现象预测正确的是 ( )

A.实验I:振荡后静置,上层溶液颜色保持不变
B.实验II:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去
C.实验III:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色
D.实验IV:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com