
| A. | N2的电子式: | B. | K+的结构示意图: | ||
| C. | H2O2的电子式: | D. | CO2的结构式O=C=O |
分析 A.氮气分子中存在氮氮三键,氮氮三建的表示方法错误;
B.钾离子的最外层达到8电子稳定结构,最外层含有18个电子;
C.双氧水为共价化合物,不存在阴阳离子;
D.二氧化碳分子中存在两个碳氧双键,为直线型结构.
解答 解:A.氮气分子中两个氮原子形成的三对共用电子对,其正确的电子式为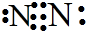 ,故A错误;
,故A错误;
B. 为钾原子结构示意图,钾离子的离子结构示意图为
为钾原子结构示意图,钾离子的离子结构示意图为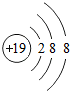 ,故B错误;
,故B错误;
C.H2O2分子为共价化合物,电子式中不存在括号和电荷,H2O2分子的电子式为 ,故C错误;
,故C错误;
D.二氧化碳为共价化合物,其分子中含有两个碳氧双键,则CO2的结构式为O=C=O,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、离子结构示意图、结构式等知识,明确常见化学用语的概念及书写原则为解答关键,试题培养了学生的规范答题能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 使用前要检查容量瓶是否漏水 | |
| B. | 容量瓶上标明了规格、温度和浓度 | |
| C. | 容量瓶用蒸馏水洗净后,要烘干水分后才能使用 | |
| D. | 配制好溶液后,要在容量瓶上贴上标签,保存备用 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 亚硝酸钠在漂白、电镀等方面应用广泛.现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示(部分夹持装置略).
亚硝酸钠在漂白、电镀等方面应用广泛.现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示(部分夹持装置略).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质的量(mol) 时间(min) | n(NH3) | n(O2) | n(H2O) |
| 0 | 2.00 | 2.25 | 0 |
| 第2min | 1.80 | 2.00 | 0.30 |
| 第4min | 1.60 | 1.75 | 0.60 |
| 第6min | 1.00 | 1.00 | 1.50 |
| 第8min | 1.00 | 1.00 | 1.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CCl4可由CH4制得,可萃取碘水中的碘 | |
| B. | 乙酸分子中含有羧基,乙酸的酸性比碳酸弱 | |
| C. | 乙醇、乙酸都能发生酯化反应 | |
| D. | 只用水就能鉴别苯和四氯化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  从Mg(OH)2悬浊液中分离出Mg(OH)2 | B. |  除去Cl2中的HCl | ||
| C. |  实验室制氨气 | D. |  排水法收集NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水、氯化钾、胆矾 | |
| B. | 液溴、水和冰混合、澄清石灰水 | |
| C. | 氮气、净化后的空气、氧化镁 | |
| D. | 白鳞、生锈的铁钉、高锰酸钾充分加热后的剩余固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com