
�������ӷ���ʽ��д��ȷ���� (����)��
A��Fe3O4��������ϡHNO3��3Fe3O4��28H����NO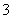 ===9Fe3����NO����14H2O
===9Fe3����NO����14H2O
B����ʳ����������̼��� �Ĵ��ڣ�CaCO3��2H��===Ca2����CO2����H2O
�Ĵ��ڣ�CaCO3��2H��===Ca2����CO2����H2O
C��FeCl2������Һ���ڿ����б��ʣ�2Fe2����4H����O2===2Fe3����2H2O
D�����MgCl2ˮ��Һ�����ӷ���ʽ��2Cl����2H2O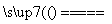 H2����Cl2����2OH��
H2����Cl2����2OH��
 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ƺ�����������е� �� �����ʷ�Ӧ������������Ȼ����ֻ����_________̬���ڡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���н�����ʵ�ķ���ʽ����ȷ���ǣ� ��
A����0.1mol/L��ˮ��pHΪ11��NH3·H2O NH4++OH-
NH4++OH-
B����Na�����ˮ�У��������壺2Na+2H2O=2NaOH +H2��
+H2��
C����CuCl2��Һ������ʵ�飬���ݷ��⣺CuCl2 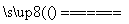 Cu2++2Cl-
Cu2++2Cl-
D��AlƬ����NaOH��Һ�У��������壺2Al+2OH-+2H2O=2AlO2-+3H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з�Ӧ�����ӷ���ʽ��д��ȷ���� (����)
A������������ʵ���Ũ�ȵ�����������Һ��̼�������Һ��ϣ�
Ba 2����2OH����NH
2����2OH����NH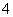 ��HCO
��HCO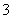 =BaCO3����NH3·H2O��H2O
=BaCO3����NH3·H2O��H2O
B���������������������Һ��Fe(OH)3��3H��=Fe3����3H2O
C��������������Һ�м����������SO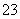 ��2H��=SO2����H2O
��2H��=SO2����H2O
D����AgNO3��Һ�м�������İ�ˮ��Ag����NH3·H2O=AgOH����NH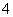
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з�Ӧ�����ӷ���ʽ��д��ȷ���� (����)��
A����Al��Ͷ��NaOH��Һ�У�Al��OH����H2O=AlO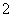 ��H2��
��H2��
B��ͭ����ϡ�����У�Cu��4H����2NO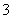 =Cu2����2NO2����2H2O
=Cu2����2NO2����2H2O
C��̼�������Һ�м������������������Һ��HCO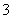 ��OH��=CO
��OH��=CO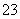 ��H2O
��H2O
D����̼������Һ����μ�����֮����������ʵ���Ũ�ȵ�ϡ���
CO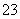 ��CH3COOH=CH3COO����HCO
��CH3COOH=CH3COO����HCO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������������һ�������²��ܴ������棬���������ӷ���ʽ��˵�����ܹ���ԭ�����(����)
| ѡ�� | ���� | ������ | ���������������ӷ�Ӧ����ʽ |
| A | pH��1����Һ | Fe2����Al3����Cl����MnO4�� | 10Cl����2MnO4����16H��===2Mn2����5Cl2����8H2O |
| B | ������c(OH)����10��2mol·L��1�������������Ӧ�ų���������Һ | K����NO3����Cl����NH4�� | NH4����OH��===NH3·H2O |
| C | ��ʹ��̪��Һ������Һ | Na����Cl����S2����SO32�� | SO32����2S2����6H��===3S����3H2O |
| D | ���д���H��������Һ | Na����Cu2����AlO2����SiO32�� | 2H����SiO32��===H2SiO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NAΪ����٤��������ֵ������˵����ȷ����
A��1.6g�������ͳ�����ɵĻ�����к�����ԭ�ӵ���ĿΪ0.1NA
B��0.1mol��ϩ���к���˫������ĿΪ0.1NA
C����״���£�11.2L���к��з��ӵ���ĿΪ0.5NA
D���� ����������ˮ�ķ�Ӧ�У�ÿ����0.1mol������ת�Ƶ��ӵ���ĿΪ0.4NA
����������ˮ�ķ�Ӧ�У�ÿ����0.1mol������ת�Ƶ��ӵ���ĿΪ0.4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������������ܽ�ij��Һ�����ʵ���Ũ�ȼ����������(����)
��ÿ10 mL��Һ�к���0.23 g Na������������Һ
��ÿ10��ˮ����������1��Na����NaOH��Һ
��Ũ��Ϊ18.4 mol·L��1������10 mL�ӵ�100 mLˮ�����õ�ϡ����
�ܱ�״���£�100 mL��������20 mLˮ��������Һ���ܶ�Ϊ0.9 g·cm��3�İ�ˮ
A���٢ڡ�������������B���٢�
C���٢� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���û�ѧ��Ӧԭ���о�Ԫ�ؼ��仯����ķ�Ӧ����Ҫ���塣
��1�����������У�SO2����������SO3��2SO2(g)�� O2(g) 2SO3(g)�������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ��ʾ���������κ�һ�㶼��ʾƽ��״̬��������ͼʾ�ش��������⣺
2SO3(g)�������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ��ʾ���������κ�һ�㶼��ʾƽ��״̬��������ͼʾ�ش��������⣺
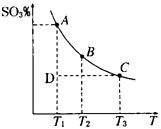
��2SO2(g) + O2(g) 2SO3(g)�ġ�H____0(�>������<��)�����ں��¡���ѹ������������ƽ����ϵ��ͨ�뺤����ƽ�� �ƶ�����������ҡ����ƶ����� ��
2SO3(g)�ġ�H____0(�>������<��)�����ں��¡���ѹ������������ƽ����ϵ��ͨ�뺤����ƽ�� �ƶ�����������ҡ����ƶ����� ��
�����¶�ΪT1ʱ����Ӧ���е�״̬Dʱ��V��_______V�����>����<����=����
��2�����ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ����������Ҫ���á�
�� ��ͼ��һ�����¶Ⱥ�ѹǿ��N2��H2��Ӧ����lmolNH3�����������仯ʾ��ͼ����д����ҵ�ϳɰ����Ȼ�ѧ����ʽ������H�ú���ĸQ1��Q2�Ĵ���ʽ��ʾ�� ��
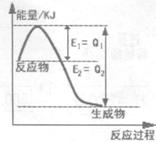
����AlCl3��Һ�еμӰ�ˮ����Ӧ�����ӷ���ʽΪ�� ��
��3����ˮ�к��д�����Ԫ�أ�����Ԫ�����ȡ���Ԫ������ں�ˮ�о��Ի���̬���ڡ���25���£���0.1mol•L��1��NaCl��Һ����μ���������0.1mol•L��1��������Һ���а�ɫ�������ɣ���Ӧ�����Һ�У���������0.1mol•L��1��NaI��Һ�������������� ȫƷ��ѧ���� �ú��벻�ˣ��������������ԭ���ǣ������ӷ���ʽ��ʾ���� ��
ȫƷ��ѧ���� �ú��벻�ˣ�����֪25��ʱKsp[AgCl] =1.0��10-10 mol2•L��2��Ksp[AgI] =1.5��10-16mol2•L��2 ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com