
| A. | 由于Ksp(ZnS)>Ksp(CuS),所以ZnS在一定条件下可转化为CuS | |
| B. | 已知AgCl的Ksp=1.8×10-10,将0.01 mol•L-1KCl溶液和等体积的0.01 mol•L-1 AgNO3溶液混合,有AgCl沉淀析出 | |
| C. | 常温下,为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH,若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 | |
| D. | pH=8的Ba(OH)2溶液和pH=8的氨水中,由水电离的c(OH-)均为1×10-8 mol•L-1 |
分析 A.从难溶电解质的转化的角度分析;
B.如生成沉淀,应满足Qc>Ksp;
C.如HA-电离大于水解,溶液呈酸性,不能说明H2A是强酸;
D.pH=8的Ba(OH)2溶液和pH=8的氨水,c(OH-)=1×10-6 mol•L-1,则水的电离程度相同.
解答 解:A.化学反应可向Ksp小的方向进行,因Ksp(ZnS)>Ksp(CuS),ZnS浊液中加入硫酸铜溶液,可转化为CuS沉淀,故A正确;
B.将0.01 mol•L-1KCl溶液和等体积的0.01 mol•L-1 AgNO3溶液混合,浓度都减小为原来的一半,则5×10-3×5×10-3>1.8×10-10,可生成沉淀,故B正确;
C.如HA-电离大于水解,溶液呈酸性,不能说明H2A是强酸,如H2SO3,故C错误;
D.pH=8的Ba(OH)2溶液和pH=8的氨水,c(OH-)=1×10-6 mol•L-1,则水的电离程度相同,则由水电离的c(OH-)均为1×10-8 mol•L-1,故D正确.
故选C.
点评 本题综合考查难容电解质的溶解平衡以及弱电解质电离,为高频考点,侧重于学生的分析、计算能力的考查,注意把握平衡移动的特点以及计算方法,难度不大.


科目:高中化学 来源: 题型:解答题
时间 浓度 | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |

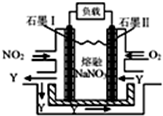
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 酸 | 醋酸 | 次氯酸 | 亚硝酸 |
| 电离常数 | 1.7×10-5 | 3.0×10-8 | 7.1×10-4 |
| A. | pH相同的氯水和亚硝酸溶液中水电离的c(H+)相同 | |
| B. | 向氯水中滴加氢氧化钠溶液至中性:c(Na+)=2 c(ClO-)+c(HClO) | |
| C. | 向漂白粉溶液中滴加H2SO3溶液可增强其漂白能力 | |
| D. | pH相同的醋酸钠、次氯酸钠和亚硝酸钠溶液中,c(Na+)最大的是亚硝酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
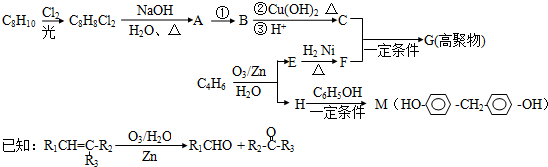
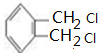
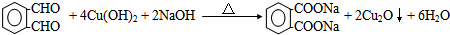
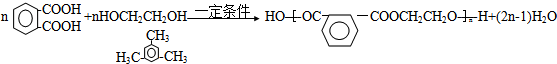
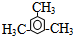 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由①只能确定溶液中有Al3+、Mg2+,没有HCO3- | |
| B. | 由②知溶液中有SO42-,没有Ba2+ | |
| C. | 由③确定溶液中有Na+,没有K+ | |
| D. | 若检验溶液中是否有存在Cl-,可取少许原溶液,直接向其中加入AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 草酸二苯酯的分子式是C14H10O4 | |
| B. | 上述变化证明化学能可以转化为光能 | |
| C. | C2O4的结构简式 | |
| D. | 反应①属于酯水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
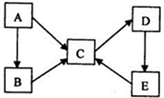 己知X、Y、Z、W为短周期四种常见元素,其中X是原子半径最小的元素,Y原子的最外层电子数是内层电子数二倍,Z能和X形成两种常见的液态化合物,W元素的单质既能与盐酸反应也能与NaOH溶液反应.元素Q是地壳中含量第二位的金属元素.试回答下列问题:
己知X、Y、Z、W为短周期四种常见元素,其中X是原子半径最小的元素,Y原子的最外层电子数是内层电子数二倍,Z能和X形成两种常见的液态化合物,W元素的单质既能与盐酸反应也能与NaOH溶液反应.元素Q是地壳中含量第二位的金属元素.试回答下列问题: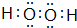 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
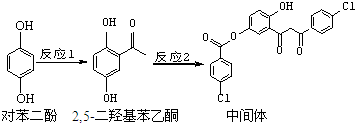
| A. | 对苯二酚在空气中能稳定存在 | |
| B. | 1 mol该中间体最多可与11 mol H2反应 | |
| C. | 2,5-二羟基苯乙酮能发生加成、水解、缩聚反应 | |
| D. | 该中间体分子中含有1个手性碳原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com