
分析 (1)根据溶液稀释前后物质的量不变计算所需浓硫酸的体积:
(2)容量瓶使用过程中需要上下颠倒,为防止漏水,使用前应检查是否漏水;容量瓶为配制一定物质的量浓度、特定体积溶液的专用仪器,不能用来溶解固体、稀释浓溶液;
(3)依据用浓溶液配制一定物质的量浓度稀溶液的一般操作步骤排序.
解答 解:(1)根据稀释定律,稀释前后溶质的物质的量不变,来计算浓硫酸的体积,设浓硫酸的体积为xmL,所以xmL×9mol/L=100mL×0.9mol/L,解得:x≈10.0.
所需浓硫酸的体积为10.0mL.
故答案为:10.0.
(2)A.容量瓶使用过程中需要上下颠倒,为防止漏水,使用前应检查是否漏水,故A正确;
B.容量瓶不能用来溶解固体,故B错误;
C.容量瓶不能用来稀释浓溶液,故C错误;
故选:A;
(3)用浓溶液配制一定物质的量浓度稀溶液的一般操作步骤:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶等,所以正确的操作顺序为:ADECBHGF;
故答案为:ADECBHGF.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理及操作步骤是解题关键,注意容量瓶构造及使用方法和注意事项,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{8b-3a}{2v}$mol/L | B. | $\frac{8b-3a}{4v}$mol/L | C. | $\frac{8b-3a}{v}$mol/L | D. | $\frac{a-2b}{2v}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
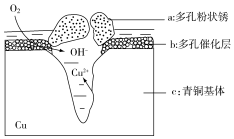 青铜器的制造是中华民族劳动人民智慧的结晶,成为一个时代的象征,但出土的青铜器大多受到环境腐蚀.如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.环境中的 Cl- 扩散到孔口,并与各电极产物作用生成多孔粉状锈 Cu2(OH)3Cl.下列说法不正确的是( )
青铜器的制造是中华民族劳动人民智慧的结晶,成为一个时代的象征,但出土的青铜器大多受到环境腐蚀.如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.环境中的 Cl- 扩散到孔口,并与各电极产物作用生成多孔粉状锈 Cu2(OH)3Cl.下列说法不正确的是( )| A. | 腐蚀过程中,负极c被氧化 | |
| B. | 环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为2Cu2++3OH-+Cl-═Cu2(OH)3Cl↓ | |
| C. | 若生成 2.145 g Cu2(OH)3Cl,则理论上消耗标准状况氧气体积为 0.448 L | |
| D. | 正极的电极反应式为:O2+4e-+2H2O═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com