
如何用密度为 ,质量分数为98%的浓硫酸来配制
,质量分数为98%的浓硫酸来配制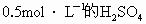 溶液500mL?简述配制过程.
溶液500mL?简述配制过程.
|
①计算:设需浓  的体积为V.则有: 的体积为V.则有:
解得 V=13.6mL.②量取:用 20mL的量筒小心地量取13.6mL的浓 . .
③溶解:向 250mL烧杯中注入约100mL蒸馏水,把量取的浓硫酸慢慢沿烧杯壁注入蒸馏水中,同时不断用玻璃棒搅拌.冷却至室温.④移液:将烧杯中的溶液用玻璃棒小心地引流到 500mL的容量瓶中.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将每次洗涤的溶液都用玻璃棒引流到容量瓶中.⑤定容:继续向容量瓶中水至离刻度线 1~2cm,振荡后改用胶头滴管滴加蒸馏水到溶液的凹液面正好与刻度线相切,再将容量瓶塞盖好,反复上下颠倒、摇匀,即得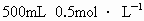 的稀硫酸溶液. 的稀硫酸溶液.
配制过程遵从一定物质的量浓度溶液配制的基本步骤.此题中的溶质源于液体浓硫酸,故先应计算出所需浓  的体积.溶解时要注意只能将浓硫酸缓慢地倒入水中稀释,以防放热发生飞溅,放冷后再转移到容量瓶中. 的体积.溶解时要注意只能将浓硫酸缓慢地倒入水中稀释,以防放热发生飞溅,放冷后再转移到容量瓶中. |


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源:物理教研室 题型:058
在一定温度下,某饱和氢氧化钠溶液体积为VmL,溶液密度为 ,质量分数为w%,物质的量浓度为
,质量分数为w%,物质的量浓度为![]() ,溶液中含氢氧化钠质量为mg.
,溶液中含氢氧化钠质量为mg.
(1)用w来表示该温度下氢氧化钠的溶解度(S)为____________.
(2)用m、V表示容器中溶质的物质的量浓度(c)为_____________.
(3)用w、d表示溶液中溶质的物质的量浓度(c)为___________.
(4)用c、d表示溶液中溶质的质量分数为__________.
查看答案和解析>>
科目:高中化学 来源: 题型:
(2)有以下物质:①16 g CH4 ②0.5 mol O2 ③5.6 L SO2 ④7 g N2 ⑤1 mol CO ⑥11.2 L C2H4(乙烯)(气体均为标准状况下的体积),则:
①质量相同的是__________________________。
②物质的量相同的是__________________________。
③相同状况下密度相同的是________________________。
④相同状况下体积最大的是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)今有N2、CO2和CO组成的混合气体,其密度是同温同压下氢气密度的16倍,则该混合气体中CO2的体积分数为_________,质量分数为_________。将上述混合气体通过加热的足量CuO后所得气体的密度在同温同压下比原混合气体密度_________(填“不变”“增大”或“减小”)。
(2)有以下物质:①16 g CH4 ②0.5 mol O2 ③5.6 L SO2 ④7 g N2 ⑤1 mol CO ⑥11.2 L C2H4(乙烯)(气体均为标准状况下的体积),则:
①质量相同的是__________________________。
②物质的量相同的是__________________________。
③相同状况下密度相同的是________________________。
④相同状况下体积最大的是_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com