
 或
或 .
. .
. +NaOH$→_{△}^{H_{2}O}$NaBr+
+NaOH$→_{△}^{H_{2}O}$NaBr+ ,其反应类型为取代反应.
,其反应类型为取代反应. (或
(或 ).
). 、
、 、
、 .
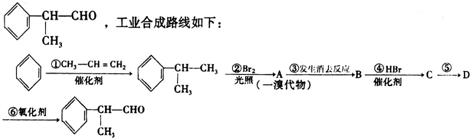
.分析 由异丙苯的结构可知,B与丙烯发生加成反应生成异丙苯,异丙苯在光照条件下 与溴发生一溴取代生成A为
与溴发生一溴取代生成A为 或
或 ,A发生消去反应生成B,则B为
,A发生消去反应生成B,则B为 ,B与HBr发生加成反应生成C,C反应生成D,D氧化生成
,B与HBr发生加成反应生成C,C反应生成D,D氧化生成 ,应是D中的羟基被氧化为醛基,逆推可得D为
,应是D中的羟基被氧化为醛基,逆推可得D为 ,则C为
,则C为 ,据此进行解答.
,据此进行解答.
解答 解:由异丙苯的结构可知,B与丙烯发生加成反应生成异丙苯,异丙苯在光照条件下 与溴发生一溴取代生成A为
与溴发生一溴取代生成A为 或
或 ;A发生消去反应生成B,则B为
;A发生消去反应生成B,则B为 ,B与HBr发生加成反应生成C,C反应生成D,D氧化生成
,B与HBr发生加成反应生成C,C反应生成D,D氧化生成 ,应是D中的羟基被氧化为醛基,逆推可得D为
,应是D中的羟基被氧化为醛基,逆推可得D为 ,则C为
,则C为 ,
,
(1)由上述分析可知,A的结构简式可能为: 或
或 ,
,
故答案为: 或
或 ;
;
(2)D的结构简式为: ,含有羟基,可以发生消去反应、取代反应,不能发生水解反应与加聚反应,所以cd正确,
,含有羟基,可以发生消去反应、取代反应,不能发生水解反应与加聚反应,所以cd正确,
故答案为:cd;
(3)B为 ,其分子中含有碳碳双键,则B可以发生加聚反应可生成高分子化合物:
,其分子中含有碳碳双键,则B可以发生加聚反应可生成高分子化合物: ,
,
故答案为: ;
;
(4)C→D的反应是卤代烃发生水解反应生成醇,也属于取代反应,化学反应方程式为: +NaOH$→_{△}^{H_{2}O}$NaBr+
+NaOH$→_{△}^{H_{2}O}$NaBr+ ,其反应类型为取代反应,
,其反应类型为取代反应,
故答案为: +NaOH$→_{△}^{H_{2}O}$NaBr+
+NaOH$→_{△}^{H_{2}O}$NaBr+ ;取代反应;
;取代反应;
(5)龙葵醛中含有-CHO,利用银镜反应或与新制氢氧化铜反应检验,化学反应方程式为: 或
或 ,
,
故答案为: (或
(或 );
);
(6)龙葵醛有多种同分异构体,符合下列条件的同分异构体:①其分子中没有甲基;②与饱和溴水反应能生成白色沉淀且与Br2的物质的量之比为1:3,所以满足条件的异构体为: 、
、 、
、 ,
,
故答案为: 、
、 、
、 .
.
点评 本题考查有机物的推断,题目难度中等,注意充分利用有机物的结构与反应条件进行推断,明确常见有机物结构与性质为解答关键,试题侧重考查学生的分析、理解能力及逻辑推理能力.


科目:高中化学 来源: 题型:解答题
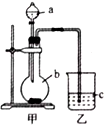 某同学想通过比较元素的最高价氧化物对应的水化物的酸性强弱来证明硫和碳的得电子能力强弱,设计了如图所示装置进行探究.
某同学想通过比较元素的最高价氧化物对应的水化物的酸性强弱来证明硫和碳的得电子能力强弱,设计了如图所示装置进行探究.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2、CH4在负极失去电子,发生氧化反应 | |
| B. | 从产物推断,两种燃料电池的氧化剂均为O2 | |
| C. | 燃料电池将化学能直接转变为电能,能量转化率高 | |
| D. | 分别将1 mol H2与1 mol CH4做燃料电池的燃料,转移的电子一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2和H2全部转化为NH3 | |
| B. | 正反应和逆反应的化学反应速率均为零 | |
| C. | N2、H2和NH3的物质的量浓度之比为1:3:2 | |
| D. | 若外界条件发生改变,化学反应的限度可能随之改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2的熔点比CO2高 | |
| B. | SiO2用于制光导纤维,干冰用于人工降雨 | |
| C. | 都能与水反应生成相应的酸 | |
| D. | 都能与强碱溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,其反应方程式为
,其反应方程式为 (不要求标出反应条件).
(不要求标出反应条件). (不要求标出反应条件).
(不要求标出反应条件).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 产品标准 | GZ5461 |
| 产品等级 | 一级 |
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体硅可用于制作光导纤维 | B. | 过氧化钠可作潜水艇中的供氧剂 | ||
| C. | 氢氟酸可用来刻蚀玻璃 | D. | 漂白粉可用作游泳池的消毒剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com